ņä£ ļĪĀ
ĒåĀļ¦łĒåĀĒÖ®ĒÖöņ×Äļ¦Éļ”╝ļ░öņØ┤ļ¤¼ņŖż(Tomato yellow leaf curl virus, TYLCV)ļŖö GeminiviridaeĻ│╝ BegomovirusņåŹņŚÉ ņåŹĒĢśļŖö single-stranded DNA ļ░öņØ┤ļ¤¼ņŖżļĪ£(Brown ļō▒, 2015), ņĄ£ņåī 11Ļ░£ņØś Ļ│äĒåĄņØ┤ ļ│┤Ļ│ĀļÉśņ¢┤ ņ׳ļŖöļŹ░(Fauquet ļō▒, 2008), 1964ļģä ņØ┤ņŖżļØ╝ņŚśņŚÉņä£ ņ▓śņØī ļČäļ”¼ļÉ£ TYLCV ļČäļ”¼ņŻ╝(TYLCV-IL)ļŖö ņĀä ņäĖĻ│äņĀüņ£╝ļĪ£ ļ░£ņāØļÉśĻ│Ā ņ׳ņ£╝ļ®░ ņŗ¼Ļ░üĒĢ£ Ļ▓ĮņĀ£ņĀü Ēö╝ĒĢ┤ļź╝ ņØ╝ņ£╝ĒéżĻ│Ā ņ׳ļŗż(CohenĻ│╝ Harpaz, 1964; CohenĻ│╝ Lapidot, 2007; Lefeuvre ļō▒, 2010; Moriones ļō▒, 2011).
TYLCVļŖö ĒåĀļ¦łĒåĀ, Ļ░Éņ×É, ļŗ┤ļ░░ ļō▒ Solanum ņåŹņŚÉ ļŗżņ¢æĒĢ£ ņ×æļ¼╝ņØä Ļ░ÉņŚ╝ņŗ£Ēéżļ®░(PolstonĻ│╝ Anderson, 1997), ĻĄŁļé┤ņŚÉņä£ļŖö Ļ░ĆļŖöņ×ÄĒĢ£ļĀ©ņ┤ł, Ēü░ļ®öĻĮā, ņćĀļ│äĻĮā ļō▒ 9Ļ│╝ 13ņóģņØś ņ×ÉņŚ░ ĻĖ░ņŻ╝ņ×Īņ┤łļź╝ Ļ░ÉņŚ╝ņŗ£Ēé¼ ņłś ņ׳ļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłļŗż(Kim ļō▒, 2012). ņØ┤ ļ░öņØ┤ļ¤¼ņŖżņŚÉ Ļ░ÉņŚ╝ļÉ£ ĒåĀļ¦łĒåĀļŖö ņ×Ä Ļ░Ćņןņ×Éļ”¼Ļ░Ć ĒÖ®ĒÖöļÉśĻ│Ā ņ×ÄņØ┤ ļ¦Éļ”¼ļŖö ņ”ØņāüņØ┤ ļéśĒāĆļéśļ®░ ļ│æņØś ņ¦äņĀäņŚÉ ļö░ļØ╝ ņŗØļ¼╝ ņĀäņ▓┤Ļ░Ć ņ£äņČĢļÉśĻ│Ā ņ┤ØņāØļÉśņ¢┤ ņØ╝ļ░śņĀüņ£╝ļĪ£ 28-92%ņØś ņłśĒÖĢļ¤ē ņåÉņŗżņØä ņØ╝ņ£╝Ēéżņ¦Ćļ¦ī, ņāØņ£Ī ņ┤łĻĖ░ ļŗ©Ļ│äņŚÉņä£ Ļ░ÉņŚ╝ļÉśļ®┤ ņłśĒÖĢņØä Ļ▒░ņØś ĒĢĀ ņłś ņŚåņ¢┤ ņĄ£ļīĆ 100% ņłśļ¤ēĻ░Éņåīļź╝ ņ┤łļלĒĢ£ļŗż(MorionesĻ│╝ Navas-Castillo, 2000; NakhlaĻ│╝ Max-well, 1998).
TYLCVļŖö ļŗ┤ļ░░Ļ░ĆļŻ©ņØ┤ņŚÉ ņØśĒĢ┤ ņśüņåŹ ņĀäņŚ╝ļÉśĻĖ░ ļĢīļ¼ĖņŚÉ ĻĖ░ņĪ┤ ļ░öņØ┤ļ¤¼ņŖż ņśłļ░®ļ▓ĢņØĆ ļ¦żĻ░£ņČ® ļ░®ņĀ£ņŚÉ ņ¦æņżæļÉśņ¢┤ņ׳ņŚłļŗż. ĻĘĖļ¤¼ļéś ĻĄŁļé┤ņŚÉ ņÜ░ņĀÉĒĢśĻ│Ā ņ׳ļŖö ļŗ┤ļ░░Ļ░ĆļŻ©ņØ┤ MED (Mediterranean)ļŖö ļäżņśżļŗłņĮöĒŗ░ļģĖņØ┤ļō£ Ļ│äĒåĄĻ│╝ insect growth regulator (IGR) Ļ│äĒåĄņØĖ Ēö╝ļ”¼ĒöäļĪØņŗ£ĒÄ£ņŚÉ ņĀĆĒĢŁņä▒ņØä ļéśĒāĆļé┤ļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłļŗż(Kim ļō▒, 2008; Lee ļō▒, 2000, 2012). ņØ┤ļĀćļō» ņĢĮņĀ£ņĀĆĒĢŁņä▒ ļ░£ļŗ¼ņØĆ ļåŹņĢĮņØś Ļ│ĀļåŹļÅä Ļ│╝ļ¤ē ņé┤Ēżļź╝ ņ£Āļ░£ĒĢ┤ ļåŹņŚģĒÖśĻ▓ĮņØä ņśżņŚ╝ņŗ£ĒéżļŖö ļō▒ņØś ļ¼ĖņĀ£ļź╝ ņĢ╝ĻĖ░ĒĢĀ ņłś ņ׳ļŗż. ļö░ļØ╝ņä£, TYLCV Ēö╝ĒĢ┤ļź╝ ņżäņØ┤ļŖö ĒÖśĻ▓Į ņ╣£ĒÖöņĀüņØĖ ļ░®ļ▓Ģņ£╝ļĪ£ ļé┤ļ│æņä▒ ĒÆłņóģ Ļ░£ļ░£Ļ│╝ ņ×æļ¼╝ņØś ņĀĆĒĢŁņä▒ ņ£ĀļÅäļ¼╝ņ¦łņØä ņØ┤ņÜ®ĒĢśļŖö ņŚ░ĻĄ¼Ļ░Ć ĒÖ£ļ░£ĒĢśĻ▓ī ņ¦äĒ¢ēļÉśĻ│Ā ņ׳ļŗż. Ēśäņ×¼Ļ╣īņ¦Ć ļé┤ļ│æņä▒ ĒåĀļ¦łĒåĀ ņ£ĪņóģņŚÉ ņé¼ņÜ®ļÉśļŖö TYLCV ļé┤ņä▒ ņ£ĀņĀäņ×ÉļŖö ņĄ£ļīĆ 6Ļ░£(Ty-1, Ty-2, Ty-3, Ty-4, Ty-5, Ty-6)ņØ┤ļ®░ S. pimpinellifolium, S. peruvianum, S. chilense, S. habrochaites ļ░Å S. cheesmaniae ļō▒ ļ¬©ļæÉ ņĢ╝ņāØĒåĀļ¦łĒåĀņŚÉņä£ ņ£ĀļלļÉśņŚłļŗż(Butterbach ļō▒, 2014; Ji ļō▒, 2007; Scott, 2007). ĻĘĖ ņżæ Ty-1ņØĆ ņāüņŚģņÜ® ĒÆłņóģņŚÉ Ļ░Ćņן ļ¦ÄņØ┤ ņé¼ņÜ®ļÉśļŖö ņ£ĀņĀäņ×ÉļĪ£ S. chilense Ļ│äĒåĄņØĖ ŌĆś LA1969ŌĆÖ (Zamir ļō▒, 1994)ņŚÉņä£ ļ│┤Ļ│ĀļÉśņŚłĻ│Ā, Ļ░ÖņØĆ ņĢ╝ņāØņóģņØś ŌĆś LA1932ŌĆÖ Ļ│äĒåĄņŚÉņä£ Ty-3, S. habrochaites Ļ│äĒåĄņØĖ ŌĆś B6013ŌĆÖņŚÉņä£ Ty-2 (Ji ļō▒, 2007; Verlaan ļō▒, 2013)Ļ░Ć ļ│┤Ļ│ĀļÉśņŚłļŗż. TYLCV ļé┤ļ│æņä▒ ĒåĀļ¦łĒåĀ ņ£ĀņĀäņ×ÉĒśĢņØĆ ņŗØļ¼╝ņ▓┤ļé┤ņŚÉņä£ ļ░öņØ┤ļ¤¼ņŖż ļ│ĄņĀ£ļź╝ ņÖäņĀäĒ׳ ņ¢ĄņĀ£ĒĢśņ¦Ć ļ¬╗ĒĢśĻ│Ā ņĀäņŗĀĻ░ÉņŚ╝ļÉśņ¢┤ Ļ▓Įļ»ĖĒĢ£ ņ”Øņāüņ£╝ļĪ£ ļ░£ĒśäļÉśĻĖ░ļÅä ĒĢśļéś Ļ░Éņłśņä▒ ņ£ĀņĀäņ×ÉĒśĢņŚÉ ļ╣äĒĢ┤ ļé«ņØĆ ņłśņżĆņØś ļ░öņØ┤ļ¤¼ņŖż ņČĢņĀüņ£╝ļĪ£ ņłśĒÖĢļ¤ē ņåÉņŗżņØä Ļ░Éņåīņŗ£Ēé©ļŗż(Lapidot ļō▒, 2001; Legarrea ļō▒, 2015).
ņĀäņŗĀĒÜŹļōØņĀĆĒĢŁņä▒(systemic acquired resistance, SAR)ņØĆ ļ│æņøÉņ▓┤ ņ╣©ņ×ģ ļō▒ņŚÉ ņØśĒĢ┤ Ēö╝ĒĢ┤ļź╝ ņ×ģņŚłņØä ļĢī ĻĘĖ Ēö╝ĒĢ┤ļź╝ ņ×ģņØĆ ļČĆņ£äļĪ£ļČĆĒä░ signalņØ┤ ņŗØļ¼╝ ņĀäņ▓┤ļĪ£ ĒŹ╝ņĀĖ ņŗØļ¼╝ņ▓┤ ņĀäņ▓┤ņŚÉ ņĀĆĒĢŁņä▒ņØ┤ ņāØĻĖ░Ļ▓ī ļÉśļŖö ĒśäņāüņØä ņØ╝ņ╗½ļŖöļŗż(Ryals ļō▒, 1996; Yalpani ļō▒, 1993). ļŗ┤ļ░░, ņĢĀĻĖ░ņןļīĆĒÆĆ ļō▒ņØś ņŗØļ¼╝ņŚÉņä£ ļ░ØĒśĆņ¦ä ļ░öņŚÉ ņØśĒĢśļ®┤, SAR ļ░£ĒśäņŚÉļŖö ņŗØļ¼╝ņ▓┤ļé┤ņØś ļ░£ļ│æĻĖ░ņĀä ļŗ©ļ░▒ņ¦ł(pathogenesis-related protein, PR protein)ņØś ņČĢņĀüņØ┤ ņ£ĀļÅäļÉśļŖöļŹ░, ņØ┤ļ¤¼ĒĢ£ PR ņ£ĀņĀäņ×É ļ░£ĒśäņØś ĒÖ£ņä▒ĒÖö ļ░Å SAR ļ░śņØæņØĆ ņé┤ļ”¼ņŗżņé░(salicylic acid, SA)ņØ┤ ļ¦żĻ░£ĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż. ņÖĖņāØ SA ņ▓śļ”¼ļŖö ņŗØļ¼╝ņØś ņāØļ¼╝ņĀü, ļ╣äņāØļ¼╝ņĀü ĒÖśĻ▓Įļ│ĆĒÖöņŚÉ ļīĆĒĢ£ ņĀĆĒĢŁņä▒ņØä ņ”ØļīĆņŗ£Ēé¼ ļ┐Éļ¦ī ņĢäļŗłļØ╝(Esmailzadeh ļō▒, 2008; Javaheri ļō▒, 2012; Khan ļō▒, 2015, 2019; Koo ļō▒, 2020), ĒĢŁļ░öņØ┤ļ¤¼ņŖż ĒÖ£ņä▒ļÅä Ē¢źņāüņŗ£ĒéżļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłļŗż(Calil Ļ│╝ Fontes, 2017; Li ļō▒, 2017, 2018). ĒåĀļ¦łĒåĀ ņ×ÄņŚÉ SAļź╝ 0.1 mM ņØś ļåŹļÅäļĪ£ ņ▓śļ”¼ĒĢśņśĆņØä ļĢī ņśżņØ┤ļ¬©ņ×ÉņØ┤Ēü¼ļ░öņØ┤ļ¤¼ņŖż(Cucumber mosaic virus, CMV), ļŗ┤ļ░░ļ¬©ņ×ÉņØ┤Ēü¼ļ░öņØ┤ļ¤¼ņŖż(Tobacco mosaic virus, TMV) ļ░Å ņł£ļ¼┤ņŻ╝ļ”äļ░öņØ┤ļ¤¼ņŖż(Turnip crinkle virus, TCV)ņØś ļ│ĄņĀ£ļź╝ ņ¢ĄņĀ£ĒĢśņśĆĻ│Ā ļŗ┤ļ░░ņØś CMV Ļ░ÉņŚ╝ņØä ņ¦ĆņŚ░ņŗ£ņ╝░ļŗż(FaoroĻ│╝ Gozzo, 2015; Shang ļō▒, 2011). SAĻ░Ć ļ░öņØ┤ļ¤¼ņŖż ļ│ĄņĀ£, ņäĖĒż Ļ░ä ņØ┤ļÅÖ ļ░Å ņןĻ▒░ļ”¼ ņłśņåĪņØä ĒżĒĢ©ĒĢ£ ļ░öņØ┤ļ¤¼ņŖż Ļ░ÉņŚ╝Ļ│╝ņĀĢņØś ņäĖ Ļ░Ćņ¦Ć ņŻ╝ņÜö ļŗ©Ļ│äņŚÉņä£ Ļ░äņäŁ ĒĢĀ ņłś ņ׳ļŗżļŖö Ļ▓āņØ┤ ļŗżļźĖ ņŚ¼ļ¤¼ ņŚ░ĻĄ¼ļź╝ ĒåĄĒĢ┤ ņ×ģņ”ØļÉśņŚłļŗż(Tahmasebi ļō▒, 2011). ņÖĖņāØ SA ņÖĖņŚÉļÅä ļŗżņ¢æĒĢ£ ņŗØļ¼╝ņČöņČ£ļ¼╝ņØ┤ ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ļĪ£ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ņ£╝ļ®░, ĻĘĖ ņżæ Ļ│äĒö╝ņśżņØ╝ņØś ņŻ╝ņÜö ĒÖ£ņä▒ ņä▒ļČäņØĖ ņ£ĀņĀ£ļåĆ(eugenol, EG)ņØĆ ņé░ĒÖöņ¦łņåī(nitric oxide, NO)ņÖĆ SA ņČĢņĀüņØä ļåÆņŚ¼ ĒåĀļ¦łĒåĀ ņŗØļ¼╝ņŚÉņä£ TYLCVņŚÉ ļīĆĒĢ£ ņĀĆĒĢŁņä▒ņØä ņ£ĀļÅäĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż(Sun ļō▒, 2016; WangĻ│╝ Fan, 2014). Tsai ļō▒(2019)ņØś ņŗżĒŚśņŚÉņä£ ĒåĀļ¦łĒåĀņŚÉ 200 ╬╝ g/ml EG ņĀäņ▓śļ”¼ļŖö TYLCV ļ░£ņāØļźĀņØä 60%Ļ╣īņ¦Ć Ļ░Éņåīņŗ£ņ╝░ļŗż. ĒéżĒåĀņé░(chitosan, CH)ņØĆ N-acetyl-D-glucosamineņØ┤ ╬▓-(1ŌåÆ4) glycosidic linage Ļ▓░ĒĢ®ņ£╝ļĪ£ ņŚ░Ļ▓░ļÉ£ ņ▓£ņŚ░ Ļ│ĀļČäņ×É ĒÖöĒĢ®ļ¼╝ļĪ£ ņāłņÜ░, Ļ▓ī, Ļ│żņČ® ļō▒ Ļ░æĻ░üļźśņØś ņÖĖĻ│©Ļ▓®Ļ│╝ ņ¦äĻĘĀņØś ņäĖĒżļ▓ĮņØś ĻĄ¼ņä▒ ņÜöņåīņØĖ ĒéżĒŗ┤ņØä ĒāłņĢäņäĖĒŗĖĒÖöĒĢśņŚ¼ ņ¢╗ņ¢┤ņ¦äļŗż(IritiĻ│╝ Varoni, 2015). ĒéżĒŗ┤Ļ│╝ CHņØś ĒīīĒÄĖņØĆ ļ»ĖņāØļ¼╝ Ļ░ÉņŚ╝ņŚÉ ļīĆĒĢ£ ļ░śņØæņ£╝ļĪ£ ņŗØļ¼╝ņŚÉņä£ ļŗżņ¢æĒĢ£ ļ░®ņ¢┤ ļ░śņØæņØä ņ£ĀļÅäĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ņ£╝ļ®░, ņŻ╝ļĪ£ ņ×ÉņŖżļ¬©ļäżņØ┤ĒŖĖ(jasmonate) ņāØĒĢ®ņä▒ņØä ņ£ĀļÅäĒĢśņŚ¼ ņĀĆĒĢŁņä▒ ņ£ĀņĀäņ×É ļ░£ĒśäņØä ņĪ░ņĀłĒĢ£ļŗż(Doares ļō▒, 1995). ņØ┤ņĀä ņŚ░ĻĄ¼ņŚÉ ļö░ļź┤ļ®┤, ņĮ®ņ×ÄņŚÉ 0.1% CH ņĀäņ▓śļ”¼ļŖö ņĢīĒīöĒīīļ¬©ņ×ÉņØ┤Ēü¼ļ░öņØ┤ļ¤¼ņŖż(Alfalfa mosaic virus, AMV)ņŚÉ ņØśĒĢ£ ĻĄŁļČĆļ│æļ░ś ņāØņä▒ņØä ņ░©ļŗ©ĒĢśņśĆĻ│Ā(Pospieszny ļō▒, 1991), ļÅÖņØ╝ĒĢ£ ļåŹļÅäļĪ£ CHļź╝ ĒåĀļ¦łĒåĀņŚÉ ņ▓śļ”¼ĒĢśĻ│Ā Ļ░Éņ×ÉĻ▒ĆņŁēļ░öņØ┤ļĪ£ņØ┤ļō£(Potato spindle tuber viroid, PSTVd)ļź╝ ņĀæņóģĒĢ£ ņŗżĒŚśņŚÉņä£ļÅä ņØ┤ņÖĆ ņ£Āņé¼ĒĢ£ ņ¢ĄņĀ£ĒÜ©Ļ│╝ļź╝ ļéśĒāĆļé┤ņŚłļŗż(Pospiezny, 1997). Mishra ļō▒(2014)ņŚÉņä£ļŖö CHļź╝ Pseudomonas ņåŹņØś ĻĘ╝ĻČīļ»ĖņāØļ¼╝Ļ│╝ Ēś╝ĒĢ®ņ▓śļ”¼ĒĢśņśĆņØä ļĢī ĒåĀļ¦łĒåĀņØś ņāØņ£ĪņØä ņ”Øņ¦äņŗ£ĒéżĻ│Ā, Tomato leaf curl virus (ToLCV) ņ¦łļ│æņØś ņżæņ”ØļÅäļź╝ 80-90% Ļ░Éņåīņŗ£ĒéżļŖö ĒÜ©Ļ│╝ļź╝ ĒÖĢņØĖĒĢśņśĆļŗż. ņØ┤ļĀćļō» ļŗżņłśņØś ņŚ░ĻĄ¼ļź╝ ĒåĄĒĢ┤ TYLCVņŚÉ ļīĆĒĢ£ ņÖĖņāØ SA, EG, CHņØś ļ░®ņĀ£ĒÜ©Ļ│╝Ļ░Ć ņ×ģņ”Ø ļÉśņŚłņØīņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ņĢäņ¦üĻ╣īņ¦Ć ņŗżņĀ£ĒżņןņŚÉņä£ ļ░öņØ┤ļ¤¼ņŖżļ│æ ļ░®ņĀ£ ņåīņ×¼ļĪ£ ņĀüņÜ®ļÉ£ ņé¼ļĪĆĻ░Ć ļČĆņĪ▒ĒĢśņŚ¼ ļäÉļ”¼ ņé¼ņÜ®ļÉśņ¦Ć ļ¬╗ĒĢśĻ│Ā ņ׳ļŗż. ļö░ļØ╝ņä£, ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ĒåĀļ¦łĒåĀņŚÉ ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ 3ņóģņØä ņ▓śļ”¼ĒĢśņśĆņØä ļĢī TYLCVņŚÉ ļīĆĒĢ£ Ļ░ÉņŚ╝ ņ¢ĄņĀ£ ĒÜ©Ļ│╝ ļ░Å ņāØņ£Ī ĒÜ©Ļ│╝ļź╝ ņŗżļé┤Ļ▓ĆņĀĢĒĢśĻ│Ā, ņŗ£ņäżĒåĀļ¦łĒåĀ ņ×¼ļ░░ ĒżņןņŚÉņä£ TYLCVņŚÉ ļīĆĒĢ£ ļ░®ņĀ£ĒÜ©Ļ│╝ļź╝ ļ╣äĻĄÉĒĢśļŖö ĒĢ£ĒÄĖ, Ļ▓ĮĻĖ░ Ļ┤æņŻ╝ņ¦ĆņŚŁņŚÉņä£ ņŻ╝ļĪ£ ņ×¼ļ░░ļÉśĻ│Ā ņ׳ļŖö ņÖäņłÖĒåĀļ¦łĒåĀ ĒÆłņóģņØś TYLCV ļé┤ņä▒ ņ£ĀņĀäņ×É ļ│┤ņ£ĀņŚ¼ļČĆļź╝ ĒÖĢņØĖĒĢśĻ│Ā, ļ░£ļ│æņĀĢļÅäļź╝ ņĪ░ņé¼ĒĢśņŚ¼ ņśüļåŹĒśäņןņŚÉņä£ ļåŹņŚģņ×Éņ×¼ ļ░Å ĒåĀļ¦łĒåĀ ĒÆłņóģ ņäĀĒāØņØä ņ£äĒĢ£ ĻĖ░ņ┤łņ×ÉļŻīļĪ£ ĒÖ£ņÜ®ĒĢśĻ│Āņ×É ĒĢśņśĆļŗż.
ņ×¼ļŻīļ░Å ļ░®ļ▓Ģ
ņŗØļ¼╝ņ×¼ļŻī ļ░Å ļ░öņØ┤ļ¤¼ņŖż ņĀæņóģ. ņŗżļé┤ ņŗżĒŚśņŚÉ ņé¼ņÜ®ĒĢ£ ĒåĀļ¦łĒåĀ ĒÆłņóģņØĆ ŌĆśņŖłĒŹ╝ļÅäĒā£ļ×æŌĆÖ (ņĮöļĀłĻ│ż)Ļ│╝ ŌĆś TYņ×ÉņØ┤ņ¢ĖņĖĀŌĆÖ (ļ»ĖĒæĖņĮö) 2ņóģņ£╝ļĪ£ 1.0% NaOClņŚÉ 1ļČä ļÅÖņĢł Ēæ£ļ®┤ņé┤ĻĘĀĒĢ£ ņóģņ×Éļź╝ ļ®ĖĻĘĀĒĢ£ Ēö╝ĒŖĖļ¬©ņŖżņÖĆ ņ¦łņäØ(1:1, w/w) Ēś╝ĒĢ®ļ¼╝ņŚÉ ĒīīņóģĒĢśņśĆļŗż. ĒīīņóģĒĢ£ ņóģņ×ÉļŖö 25┬░C ņĢöņĪ░Ļ▒┤ņŚÉņä£ ļ░£ņĢäņŗ£ņ╝£ ņ×ÉņŚĮņØ┤ ņĀäĻ░£ļÉśņŚłņØä ļĢī, Hoagland ļ░░ņ¢æņĢĪ(MBcell, Seoul, Korea)ņØä ņŻ╝ĻĖ░ņĀüņ£╝ļĪ£ Ļ┤ĆņŻ╝ĒĢśņŚ¼ 2ņŻ╝Ļ░ä ņāØņןņāüņŚÉņä£ ņŻ╝Ļ░ä 26┬░C, ņĢ╝Ļ░ä 23┬░C, Ļ┤æļÅä 185 ╬╝ mol/m2/s ņĪ░Ļ▒┤ņ£╝ļĪ£ ņ£Īļ¼śĒĢśņśĆļŗż. ļ░öņØ┤ļ¤¼ņŖż ņĀæņóģņøÉņØĆ ĻĄŁļé┤ ļ░£ņāØ TYLCV-ILņŚÉ ļīĆĒĢśņŚ¼ ņäĀĒ¢ēņŚ░ĻĄ¼(Kil ļō▒, 2014)ņŚÉņä£ ņé¼ņÜ®ĒĢ£ Ļ░ÉņŚ╝ņä▒ Ēü┤ļĪĀņØä ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░, Kil ļō▒(2014)ņØś ļ░®ļ▓ĢņŚÉ ļö░ļØ╝ ļ░░ņ¢æĒĢśņśĆļŗż. ĒśĢņ¦łņĀäĒÖśļÉ£ Agrobacterium tumefaciensļź╝ 3ņóģņØś ĒĢŁņāØņĀ£(50 ╬╝ g/ml ņØś kanamycin, 50 ╬╝g/mlņØś rifampicin, 10 ╬╝g/mlņØś genta-mycin)ļź╝ ņ▓©Ļ░ĆĒĢ£ Luria-Bertani ļ░░ņ¦ĆņŚÉņä£ 28┬░C, 24ņŗ£Ļ░ä ņ¦äĒāĢļ░░ņ¢æĒĢśņśĆļŗż. ņĀæņóģņØĆ 2-3ņŚĮĻĖ░ņŚÉ ĒåĀļ¦łĒåĀ ņżäĻĖ░ ņĀĢļŗ©ļČĆļź╝ Ļ│żņČ®ĒĢĆņØä ņØ┤ņÜ®ĒĢśņŚ¼ 10ĒÜī Ļ░Ćļ¤ē ļ░śļ│ĄĒĢśņŚ¼ ņ░öļ¤¼ņżĆ Ēøä, ļ░░ņ¢æņĢĪ 500 ╬╝ lļź╝ ņ░öļ¤¼ņżĆ ļČĆņ£äņŚÉ ņØ╝ĒÜīņÜ® ņŖżĒżņØ┤ļō£ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņĪ░ņŗ¼ņŖżļ¤ĮĻ▓ī ļ¢©ņ¢┤ļ£©ļ”¼ļ®┤ņä£ ĒØĪņłśļÉśļÅäļĪØ ĒĢśņśĆļŗż. ņĀæņóģĒĢ£ ņŗØļ¼╝ņ▓┤ļŖö ņŻ╝ņĢ╝Ļ░ä ņś©ļÅäĻ░Ć 26┬░CņÖĆ 23┬░CļĪ£ ņ£Āņ¦ĆļÉśļŖö ņāØņןņāü(Ļ┤æ/ņĢö, 16 hr/8 hr; ņŖĄļÅä, 50% ņØ┤ņāü)ņŚÉņä£ ņ×¼ļ░░ĒĢśņśĆļŗż.
ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ ņŗżļé┤Ļ▓ĆņĀĢ. ĒåĀļ¦łĒåĀ ŌĆśņŖłĒŹ╝ļÅäĒā£ļ×æŌĆÖ ĒÆłņóģņØä ĒīīņóģĒĢśņŚ¼ 3-4 ņŚĮĻĖ░ļÉ£ ņ£Āļ¼śņŚÉ SA (2-hydroxybenzoic acid 99%, Sigma-Aldrich, St. Louis, MO, USA)Ļ│╝ EG (2-methoxy-4-(2-propenyl)phenol 99%, Sigma-Aldrich), CH (poly(D-glucos-amine) 500-190 kDa, Sigma-Aldrich)ņØä ĒØśļ¤¼ļé┤ļ”┤ ņĀĢļÅäļĪ£ ņČ®ļČäĒ׳ ļČäļ¼┤ņ▓śļ”¼ĒĢśĻ│Ā, 24ņŗ£Ļ░ä ļÆż TYLCV Ļ░ÉņŚ╝ Ēü┤ļĪĀņØä ņĀæņóģ(virus infected control, VP)ĒĢśņśĆļŗż. SAĻ│╝ EG, CHņØś ņŚĮļ®┤ņé┤Ēż ļåŹļÅäļŖö ņØ┤ņĀäļ¼ĖĒŚīņØä ņ░ĖĻ│ĀĒĢśņŚ¼ Ļ░üĻ░ü 2 mM SA, 200 ╬╝ g/ml EG, 0.1% CHļĪ£ ņäĀņĀĢĒĢśņśĆļŗż(Li ļō▒, 2019; Rendina ļō▒, 2019; Sun ļō▒, 2016). ņŗżĒŚśņØĆ SAT+VP, EGT+VP, CHT+VP, VP ļ░Å ļ¼┤ņĀæņóģ(CP)ņ£╝ļĪ£ ņ┤Ø 5Ļ░£ ņ▓śļ”¼ĻĄ¼ļĪ£ ĻĄ¼ņä▒ĒĢśņśĆĻ│Ā ņŗØļ¼╝ ņāØņןņāüņŚÉņä£ ļé£Ļ┤┤ļ▓Ģņ£╝ļĪ£ ļ░░ņ╣śĒĢśņśĆņ£╝ļ®░, ņ▓śļ”¼ļŗ╣ ĒåĀļ¦łĒåĀļź╝ 12ņŻ╝ņö® 3ļ░śļ│Ąņ£╝ļĪ£ ņŗżĒŚśņØä ņ¦äĒ¢ēĒĢśņśĆļŗż. ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ 3ņóģ ņ▓śļ”¼ ļ░Å TYLCV Ļ░ÉņŚ╝ņØ┤ ĒåĀļ¦łĒåĀ ņāØņ£ĪņŚÉ ļ»Ėņ╣śļŖö ņśüĒ¢źņØä ņĪ░ņé¼ĒĢśĻĖ░ ņ£äĒĢ┤ ņ▓śļ”¼ 50ņØ╝ Ēøä Ļ░ü ņ▓śļ”¼ĻĄ¼ļ│ä ņ┤łņןĻ│╝ ņ¦ĆņāüļČĆ ļ░Å ņ¦ĆĒĢśļČĆ ņāØņ▓┤ņżæņØä ņĖĪņĀĢĒĢśņśĆļŗż. TYLCVņŚÉ ļīĆĒĢ£ ĒĢŁļ░öņØ┤ļ¤¼ņŖżĒÜ©Ļ│╝ ņĪ░ņé¼ļŖö TYLCV ņĀæņóģ 18ņØ╝ ļ░Å 32ņØ╝ Ēøä, ņ▓śļ”¼ļ│ä ĒåĀļ¦łĒåĀņŚÉ TYLCV ļ░£ļ│æļÅäļź╝ ņĪ░ņé¼ĒĢśņśĆĻ│Ā, double antibody sandwich enzyme linked immunosorbent assay (DAS-ELISA) ļ░®ļ▓Ģņ£╝ļĪ£ ļ░öņØ┤ļ¤¼ņŖż ļåŹļÅäļź╝ ļ╣äĻĄÉĒĢśņśĆļŗż. ņŗĀņ┤ł ņ×ÄņØä 0.1 gņö® ļ¼┤ņ×æņ£äļĪ£ ņ▒äņĘ©ĒĢ£ Ēøä ņČöņČ£ņĢĪ 1 mlņØä ņ▓©Ļ░ĆĒĢśĻ│Ā, zirconia beadsļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļ¦łņćäĒĢ£ Ēøä ņøÉņŗ¼ļČäļ”¼ĒĢ£ ņāüņ¦ĢņĢĪņØä ņé¼ņÜ®ĒĢśņśĆļŗż. TYLCV ĒĢŁņ▓┤ Ļ▓ĆņČ£ņÜ®ņ£╝ļĪ£ ņŗ£ĒīÉņżæņØĖ TYLCV complete kit (Bioreba, Reinach, Switzerland)ļź╝ ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░, ņĀ£ņĪ░ņé¼ņŚÉņä£ ĻČīņןĒĢśļŖö ļ░®ļ▓ĢņŚÉ ļö░ļØ╝ ņŗżņŗ£ĒĢśņśĆļŗż. ļ░öņØ┤ļ¤¼ņŖż ņĖĪņĀĢņØĆ ELISA Microplate Reader (SpectraMax 190, Molecular Devices, Sunnyvale, CA, USA)ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ 450 nm ņØś ĒīīņןņŚÉņä£ ĒØĪĻ┤æļÅäļź╝ ņĖĪņĀĢĒĢśņśĆļŗż.
ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ ĒżņןĻ▓ĆņĀĢ. ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ 3ņóģņØś ļåŹĻ░Ćņŗżņ”Ø ņŗ£ĒŚśņØĆ Ļ▓ĮĻĖ░ļÅä Ļ┤æņŻ╝ņŗ£ Ēć┤ņ┤īļ®┤ ņĀĢņ¦Ćļ”¼ņŚÉ ņ£äņ╣śĒĢ£ ļåŹĻ░Ć ĒĢśņÜ░ņŖżņŚÉņä£ ņŗżņŗ£ļÉśņŚłņ£╝ļ®░ ņ£Īļ¼śņןņŚÉņä£ ĻĄ¼ņ×ģĒĢ£ ŌĆśļÅäĒā£ļ×æņåöļØ╝ŌĆÖ (ņĮöļĀłĻ│ż) ĒÆłņóģņØś ĒåĀļ¦łĒåĀļź╝ 2020ļģä 7ņøö 3ņØ╝ņŚÉ ņĀĢņŗØĒĢśņŚ¼ 6Ļ░£ņøö ļÅÖņĢł ņŗżĒŚśņØä ņłśĒ¢ēĒĢśņśĆļŗż. ņŗżĒŚśņŚÉ ņé¼ņÜ®ļÉ£ ņ▓śļ”¼ĻĄ¼ļŖö SAT, EGT, CHT, ļ¼┤ņ▓śļ”¼(NT)ļĪ£ ņ┤Ø 4Ļ░£ļĪ£ ĻĄ¼ņä▒ĒĢśņśĆĻ│Ā, ņĀĢņŗØ ņ¦üĒøä 2 mM SA, 200 ╬╝ g/ml EG, 0.1% CHļź╝ 1ņŻ╝ņØ╝ Ļ░äĻ▓®ņ£╝ļĪ£ ņłśĒÖĢ ņ¦üņĀäĻ╣īņ¦Ć ņ┤Ø 8ĒÜī ņ¦ĆņāüļČĆļź╝ ņČ®ļČäĒ׳ ņĀüņŗżļ¦īĒü╝ ņé┤ĒżĒĢśņśĆļŗż. TYLCV Ļ░ÉņŚ╝ļźĀ ņĪ░ņé¼ļŖö ņĀĢņŗØ 30ņØ╝ ļÆżņÖĆ 90ņØ╝ ļÆżņŚÉ Ļ░üĻ░ü ņŗżņŗ£ĒĢśņśĆņ£╝ļ®░, ļ│æņ¦ĢņØś ņ£Āļ¼┤ņÖĆ ņāüĻ┤ĆņŚåņØ┤ ĒåĀļ¦łĒåĀ ņŗĀņ┤ł ņ×ÄņØä ļ¼┤ņ×æņ£äļĪ£ ņ▒äņ¦æĒĢśņŚ¼ polymerase chain reaction (PCR)ņØä ņŗżņŗ£ĒĢśņśĆļŗż. ņ▒äņ¦æĒĢ£ ņŗ£ļŻīļŖö ņ×ÉļÅÖĒĢĄņé░ņČöņČ£ņןļ╣äņØĖ magLEAD 12gC (Precision System Science Co., Matsudo, Japan)ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ total DNA/RNAļź╝ ļČäļ”¼ĒĢśņśĆĻ│Ā, TYLCV Ļ▓ĆņČ£ņØä ņ£äĒĢ┤ Lee ļō▒(2013)ņŚÉ ņØśĒĢ┤ ļ│┤Ļ│ĀļÉ£ ĒŖ╣ņØ┤ ĒöäļØ╝ņØ┤ļ©Ė TYLCV-M1F (CACGATT-TAATTAGGGATCTTATATCTG)ņÖĆ TYLCV-M1R (ATCAGGGCTTC-GATACATTC)ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ PCRņØä ņłśĒ¢ēĒĢśņśĆļŗż. ĒåĀļ¦łĒåĀņØś ņłśĒÖĢņØĆ ņĀĢņŗØ 55ņØ╝ ĒøäļČĆĒä░ ņŗ£ņ×æĒĢśņśĆĻ│Ā, 1ĒÖöļ░® ņĪ░ĻĖ░ņłśļ¤ēĻ│╝ 5ĒÖöļ░®Ļ╣īņ¦Ć ņĀäņ▓┤ ņłśļ¤ēņØä ņĖĪņĀĢĒĢśņśĆņ£╝ļ®░, ĒåĄĻ│äņ▓śļ”¼ ļČäņäØņØä ĒåĄĒĢśņŚ¼ ņ▓śļ”¼ļ│ä ņłśļ¤ēņä▒ ņ░©ņØ┤ļź╝ ļČäņäØĒĢśņśĆļŗż.
ļ░öņØ┤ļ¤¼ņŖż ņĀĆĒĢŁņä▒ Ļ▓ĆņĀĢ. Ļ░ÉņŚ╝ņä▒Ēü┤ļĪĀ TYLCV-ILņØä ņé¼ņÜ®ĒĢśņŚ¼ ĒåĀļ¦łĒåĀ ĒÆłņóģ ŌĆśņŖłĒŹ╝ļÅäĒā£ļ×æŌĆÖ ļ░Å ŌĆś TYņ×ÉņØ┤ņ¢ĖņĖĀŌĆÖņŚÉ ņĀæņóģĒĢśņśĆņ£╝ļ®░, ņĀæņóģĒĢ£ ņŗØļ¼╝ņ▓┤ļŖö ņŻ╝ņĢ╝Ļ░ä ņś©ļÅäĻ░Ć 26┬░CņÖĆ 23┬░CļĪ£ ņ£Āņ¦ĆļÉśļŖö ņāØņןņāü(Ļ┤æ/ņĢö, 16 hr/8 hr; ņŖĄļÅä, 50% ņØ┤ņāü)ņŚÉņä£ 30ņØ╝ ļÅÖņĢł ņ×¼ļ░░ĒĢśļ®┤ņä£ ļ│æņ¦ĢņØä ņĪ░ņé¼ĒĢśņśĆļŗż. ļ░öņØ┤ļ¤¼ņŖż ņĀæņóģņØĆ ĒÆłņóģ ļŗ╣ 10ņŻ╝ņö® 3ļ░śļ│Ąņ£╝ļĪ£ ņŗżņŗ£ĒĢśņśĆļŗż. ļ░öņØ┤ļ¤¼ņŖż ņĪ░ņé¼ļŖö Choi ļō▒(2013)ņØś ļ░®ļ▓ĢņØä ļ│ĆĒśĢĒĢśņŚ¼ ņ”Øņāü ņŚåņØī(0), ņĢĮĒĢ£ ņ”Øņāü(1), ĒÖ®ĒÖöņ”Øņāü(2), ņ£äņČĢĻ│╝ ĒÖ®ĒÖö ņ×Äļ¦Éļ”╝(3)ņØś 4ļŗ©Ļ│äļĪ£ ĻĄ¼ļČäĒĢśĻ│Ā ļŗżņØīĻ│╝ Ļ░ÖņØ┤ ļ░£ļ│æļÅä(ļ░£ļ│æļÅä(%)=[╬Ż(ļ░£ļ│æņłś├Śļ░£ļ│æĻ│äņłś)/3├ŚĻ░£ņ▓┤ņłś]├Ś100)ļĪ£ ĒÖśņé░ĒĢśņśĆļŗż.
TYLCV ļé┤ļ│æņä▒ ņ£ĀņĀäņ×ÉļŖö Ty1/3Ļ│╝ ņŚ░Ļ┤ĆļÉ£ cleaved amplified polymorphic sequences (CAPS) ļ¦łņ╗ż (ŌĆś TY1-SspIŌĆÖ)ņÖĆ ļé┤ņä▒ ņ£ĀņĀäņ×É Ty-2, Ty-3 ļśÉļŖö Ty-3aņÖĆ ņŚ░Ļ┤ĆļÉ£ sequence characterized amplified region (SCAR) ļ¦łņ╗ż (ŌĆś TO302ŌĆÖ, ŌĆś P6-25ŌĆÖ)ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ Ļ▓ĆņĀĢĒĢśņśĆļŗż(Table 1). Genomic DNAļŖö ĒåĀļ¦łĒåĀ ļ│Ė ņ×Ä 5-7ņŚĮĻĖ░ņŚÉ ņ×ÉļÅÖĒĢĄņé░ņČöņČ£ņŗ£ņŖżĒģ£ņØĖ magLEAD 12gCļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ļ¦żļē┤ņ¢╝ņŚÉ ļö░ļØ╝ ņČöņČ£ĒĢśņśĆļŗż. SCAR ļ¦łņ╗ż PCR ņłśĒ¢ēņØä ņ£äĒĢ┤ gDNA 2 ╬╝ lņŚÉ SCAR primer Ļ░üĻ░ü 20 pMĻ│╝ PCR ļ░śņØæņĢĪ(0.025 U KOD-FX polymerase, 0.2 mM dNTP; TOYOBO, Osaka, Japan) 20 ╬╝ l ļź╝ ņä×Ļ│Ā 94┬░CņŚÉņä£ 10ļČä pre-denatureļź╝ ņłśĒ¢ēĒĢ£ Ēøä, denature 94┬░C 30ņ┤ł, annealing 60┬░C 30ņ┤ł, extension 72┬░C 2ļČäņ£╝ļĪ£ ņ┤Ø 34 cycleļĪ£ ļ░śņØæņŗ£Ēé© Ēøä last extension 72┬░CņŚÉņä£ 5ļČäĻ░ä ņ¦äĒ¢ēņŗ£ņ╝░ļŗż. CAPS ļ¦łņ╗ż ļČäņäØņØĆ ņ”ØĒÅŁļÉ£ PCR ņé░ļ¼╝ 5 ╬╝ lļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņ┤Ø 10 ╬╝ lņØś ļ░śņØæņĢĪņŚÉ 0.5 UņØś ņĀ£ĒĢ£ĒÜ©ņåīļź╝ ņ▓śļ”¼ĒĢ£ Ēøä 1├Ś TBE buffer (Bioneer, Daejeon, Korea)Ļ░Ć ņ▓©Ļ░ĆļÉ£ 2% agarose gelņØä ņØ┤ņÜ®ĒĢśņŚ¼ 75 VņŚÉņä£ 35ļČäĻ░ä ņĀäĻĖ░ņśüļÅÖņØä ņŗżņŗ£ĒĢśņŚ¼ UV illuminationņāüņŚÉņä£ Ļ┤Ćņ░░ĒĢśņśĆļŗż.
Table┬Ā1.
Primers and reaction conditions for molecular markers linked to the TYLCV-resistance
| Primer name | Primer sequence (5ŌĆÖ-3ŌĆÖ) | Tm (oC) | Marker type | Resistant locus | Product size a (bp) R/S | Reference |
|---|---|---|---|---|---|---|
| Ty1-IY | F-ATGAAGACAAAAACTGCTTC | 55 | CAPS with SspI | Ty1/3 | 608/224, 386 | Jung et al.(2015) |
| R-TCAGGGTTTCACTTCTATGAAT | ||||||
| T0302 | F-TGGCTCATCCTGAAGCTGATAGCGC | 55 | SCAR | Ty2 | 900/800 | Yang et al. (2014) |
| R-AGTGTACATCCTTGCCATTGACT | ||||||
| P6-25 | F-GGTAGTGGAAATGATGCTGCTC | 53 | SCAR | Ty3a | 630/320 | Ji et al. (2007) |
| R-GCTCTGCCTATTGTCCCATATATAACC |
ĒåĄĻ│äļČäņäØ. ņłśņ¦æļÉ£ ņ×ÉļŻīņØś ĒåĄĻ│äļČäņäØņØĆ SPSSĒöäļĪ£ĻĘĖļש(IBM SPSS Statistics ver. 26.0, IBM Corp., Armonk, NY, USA)ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ļČäņé░ļČäņäØ(one-way analysis of variance)Ēøä Duncan ļŗżņżæ ļ▓öņ£äĻ▓ĆņĀĢ(Duncan multiple range test, 5%)ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņ£ĀņØśņä▒ņØś ņ░©ņØ┤ļź╝ Ļ▓ĆņĀĢĒĢśņśĆļŗż.
Ļ▓░Ļ│╝ļ░Å Ļ│Āņ░░
ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ ņŗżļé┤Ļ▓ĆņĀĢ. ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ 3ņóģņØś ņŚĮļ®┤ņé┤Ēż Ēøä TYLCV ņĀæņóģņØä ņłśĒ¢ēĒĢ£ Ļ▓░Ļ│╝(Table 2), TYLCVņŚÉ Ļ░ÉņŚ╝ļÉ£ ņ¦Ć 12ņØ╝ Ēøä VPņŚÉņä£ ņāØņןņĀÉņØ┤ ĒÖ®ĒÖöļÉśĻ│Ā ņ×ÄņØ┤ ļ¦Éļ”¼ļŖö ņ”ØņāüņØ┤ ļéśĒāĆļéśĻĖ░ ņŗ£ņ×æĒ¢łĻ│Ā, ņĀæņóģ 18ņØ╝ ĒøäļČĆĒä░ CPļź╝ ņĀ£ņÖĖĒĢ£ ļ¬©ļōĀ ņ▓śļ”¼ĻĄ¼ņŚÉņä£ TYLCV ņ”ØņāüņØ┤ ļ░£ĒśäļÉśņŚłļŗż. ņ▓śļ”¼ Ēøä 50ņØ╝ņ¦Ė ļ░öņØ┤ļ¤¼ņŖżļź╝ ņĀæņóģĒĢ£ ļ¬©ļōĀ ņ▓śļ”¼ĻĄ¼ņØś ņ┤łņןņØĆ CPņŚÉ ļ╣äĒĢ┤ ļé«ņĢśĻ│Ā, ņ¦ĆņāüļČĆ ņāØņ▓┤ņżæņØś Ļ▓ĮņÜ░ EGT+VPņØĆ 8.6 g, CHT+VPņØĆ 8.7 g, SAT+VPņØĆ 9.1 g, VPņØĆ 10.0 g ņł£ņ£╝ļĪ£ ļåÆņĢśļŗż. ļ│Ė ņŚ░ĻĄ¼Ļ▓░Ļ│╝ TYLCVņØś Ļ░ÉņŚ╝ņ£╝ļĪ£ ņØĖĒĢ┤ ĒåĀļ¦łĒåĀņØś ņ┤łņןņØĆ Ļ░ÉņåīĒ¢łņ¦Ćļ¦ī ņśżĒ׳ļĀż ņ¦ĆņāüļČĆ ņāØņ▓┤ņżæņØĆ ņ”ØĻ░ĆĒĢ£ Ļ▓āņ£╝ļĪ£ ļ»ĖļŻ©ņ¢┤ļ│╝ ļĢī ņŗØļ¼╝ ņ▓┤ļé┤ņŚÉ ņ╣©ņ×ģĒĢ£ ļ░öņØ┤ļ¤¼ņŖżņØś ņ×æņÜ®ņØ┤ ĒåĀļ¦łĒåĀņØś ņāØļ”¼, ņāØņןļ░śņØæņØä ļ╣äņĀĢņāüņĀüņ£╝ļĪ£ ļ│ĆĒÖöņŗ£Ēé© Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż. Seo ļō▒(2018)ņŚÉņä£ TYLCV Ļ░ÉņŚ╝ņ£╝ļĪ£ ļ░£ĒśäļÉśļŖö ņ£äņČĢ, ņÖ£ĒÖö ļō▒ņØś ļ│æņ¦ĢņŚÉļŖö ņģĆļŻ░ļĪ£ņśżņŖż ņāØĒĢ®ņä▒ Ļ▓ĮļĪ£ņÖĆ Ļ┤ĆļĀ©ļÉ£ ļŗżņ¢æĒĢ£ ņ£ĀņĀäņ×ÉĻ░Ć Ļ┤ĆņŚ¼ĒĢśļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłĻ│Ā, TYLCVņØś C4 ļŗ©ļ░▒ņ¦łņØ┤ ņŚ¼ļ¤¼ ņŗØļ¼╝ļ░£ļŗ¼ Ļ┤ĆļĀ© ņ£ĀņĀäņ×ÉņØś ņĀäņé¼ Ļ▓ĮļĪ£ļź╝ ļ░®ĒĢ┤ĒĢśņŚ¼ ņ×ÄņØś ļ¦Éļ”╝ņ”ØņāüņØä ņ£ĀļÅäĒĢśļŖö Ļ▓āņ£╝ļĪ£ ļ░ØĒśĆņĪīļŗż(CorralesŌĆÉ Gutierrez ļō▒, 2020). ļ┐Éļ¦ī ņĢäļŗłļØ╝ TYLCVļŖö ņŗØļ¼╝ ņ▓┤ļé┤ ņłśļČä ņåÉņŗżņØä ļ¦ēĻĖ░ ņ£äĒĢ┤ ņ”Øņé░ņ£©Ļ│╝ ĻĖ░Ļ│ĄņĀäļÅäļÅäļź╝ Ļ░Éņåīņŗ£ņ╝░ņ£╝ļ®░, ņØ╝ļČĆ ĒāäņłśĒÖöļ¼╝Ļ│╝ ņĢäļ»ĖļģĖņé░ ļō▒ņØś ņé╝Ēł¼ ļ│┤ĒśĖņĀ£ļź╝ ļ┐īļ”¼ļĪ£ ņ×¼ļČäļ░░ĒĢśņŚ¼ R/S (root/shoot) ļ╣äņ£©ņØä ņ”ØĻ░Ćņŗ£ņ╝░ļŗż(Mishra ļō▒, 2022; Shteinberg ļō▒, 2021).
Table┬Ā2.
The effects of growth and disease inhibition by foliar spray with antiviral compounds for TYLCV in susceptible tomato cultivar ŌĆśSuperdotaerangŌĆÖ
| Materials a | Plant height (cm) | Shoot fresh weight (g/plant) | Root fresh weight (g/plant) | Disease severity(%) | |
|---|---|---|---|---|---|
| 18 DPI | 32 DPI | ||||
| CP | 40.7 a b | 8.2 b | 0.2 bc | 0.0 c | 0.0 c |
| VP | 36.1 b | 10.0 a | 0.3 a | 78.6 a | 98.8 a |
| SAT+VP | 35.8 b | 9.1 ab | 0.3 a | 56.8 b | 98.8 a |
| CHT+VP | 34.2 bc | 8.7 ab | 0.2 bc | 59.5 b | 87.5 b |
| EGT+VP | 32.1 c | 8.6 b | 0.2 c | 55.1 b | 98.7 a |
ļö░ļØ╝ņä£, ļ│Ė ņŚ░ĻĄ¼Ļ▓░Ļ│╝ ļ░öņØ┤ļ¤¼ņŖż ņĀæņóģ ņ▓śļ”¼ĻĄ¼ņØś ņ┤łņן Ļ░ÉņåīļŖö TYLCVņØś ņĀäĒśĢņĀüņØĖ ļ│æņ¦Ģ ļ░£ĒśäņŚÉ ĻĖ░ņØĖĒĢ£ Ļ▓░Ļ│╝ņØ┤ļ®░, ņāØņ▓┤ņżæņØś ņ”ØĻ░Ć ļśÉĒĢ£ TYLCV Ļ░ÉņŚ╝ņŚÉ ļö░ļźĖ ņ▓┤ļé┤ ņé╝Ēł¼ļ│┤ĒśĖņĀ£ņØś ņČĢņĀü ļĢīļ¼ĖņØ╝ Ļ▓āņ£╝ļĪ£ ņČöņĖĪļÉ£ļŗż. ļ░śļ®┤, VPņÖĆ ļ╣äĻĄÉĒĢśņŚ¼ SAT+VP, CHT+VP, EGT+VP ņØś ņ¦ĆņāüļČĆ ļ░Å ņ¦ĆĒĢśļČĆ ņāØņ▓┤ņżæņØ┤ ņāüļīĆņĀüņ£╝ļĪ£ ļé«ņĢśļŖöļŹ░, ņØ┤ļŖö ĒĢŁļ░öņØ┤ļ¤¼ņŖż 3ņóģņØś ņ▓śļ”¼Ļ░Ć Ļ░ÉņŚ╝ņ┤łĻĖ░ ņŗØļ¼╝ņ▓┤ļé┤ SAR ņ£ĀļÅäņ×æņÜ®ņ£╝ļĪ£ ņ×Éņ▓┤ ļ░®ņ¢┤ĻĖ░ņ×æņØä ĒÖ£ņä▒ĒÖöņŗ£ņ╝£ņ£╝ļéś, ņŗØļ¼╝ ņāØņ£ĪņØĆ ņ¢ĄņĀ£ņŗ£Ēé© Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
TYLCVĻ░Ć ņ╣©ņ×ģ Ēøä ņä▒Ļ│ĄņĀüņØĖ Ļ░ÉņŚ╝ņØä ņ£äĒĢ┤ ņŗØļ¼╝ņØś Ļ│╝ļ»╝ņä▒ņäĖĒżņé¼ļ®Ėļ░śņØæ(hypersensitive cell death)ņØä ņ£ĀļÅäĒĢśņ¦Ć ņĢŖņ£╝ļ®░, ĻĖ░ņŻ╝ ņŗØļ¼╝ņØś ņāżĒÄśļĪĀ ņŚ┤ņČ®Ļ▓®ļŗ©ļ░▒ņ¦ł 90 (heat shock protein 90)ņØä ļ╣äĒÖ£ņä▒ĒÖöĒĢśĻ│Ā, ņŚ┤ņČ®Ļ▓®ņĀäņé¼ņØĖņ×É(heat shock transcription factor)ļź╝ ņ¢ĄņĀ£ĒĢśļŖö ļō▒ņØś ņŗØļ¼╝ ļ░®ņ¢┤ ļ░śņØæņØä ĒÜīĒö╝ĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż(Anfoka ļō▒, 2016). ļ░śļ®┤, SAņŚÉ ņØśĒĢ┤ ļ¦żĻ░£ļÉ£ ļ░®ņ¢┤ ļ░śņØæņØś ĒÖ£ņä▒ĒÖöļŖö ņóģņóģ ņŗØļ¼╝ņØś ņä▒ņןņØä ņ¢ĄņĀ£ĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŖöļŹ░(Huot ļō▒, 2014; Karasov ļō▒, 2017), ņØ┤ņĀäņŚÉ ļ¬ćļ¬ć ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņÖĖņāØ SAņØś ņ▓śļ”¼Ļ░Ć ņØ╝ļČĆ ņŗØļ¼╝ ņóģņŚÉņä£ ņ▓śļ”¼ ļåŹļÅäņŚÉ ļö░ļØ╝ ņśüņ¢æņä▒ņןņØä Ļ░Éņåīņŗ£ņ╝░ļŗż(Rivas-San VicenteņÖĆ Plasencia, 2011). Matricaria chamomillaņŚÉ 250 ╬╝ M SA ņ▓śļ”¼ļŖö ņ¦ĆņāüļČĆ ļ░Å ņ¦ĆĒĢśļČĆņØś ņāØņןņØä ņ¢ĄņĀ£ņŗ£ņ╝░Ļ│Ā(Kov├Īcik ļō▒, 2009), ArabidopsisņŚÉņä£ļÅä 50 ╬╝ M ļåŹļÅäņØś SA ņ▓śļ”¼Ļ░Ć ļ┐īļ”¼ ņāØņןņØä ņ¢ĄņĀ£ņŗ£Ēé©ļŗżļŖö ļ│┤Ļ│ĀĻ░Ć ņ׳ņŚłļŗż(Pasternak ļō▒, 2019).
ņ▓śļ”¼ļ│ä TYLCV ļ░£ļ│æļÅä ņĪ░ņé¼ Ļ▓░Ļ│╝ ņĀæņóģ 18ņØ╝ Ēøä VPņŚÉņä£ļŖö 78.6%ņśĆĻ│Ā, SAT+VP, CHT+VP, EGT+VPņŚÉņä£ļŖö Ļ░üĻ░ü 56.8%, 59.5%, 55.1%ļĪ£ ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ 3ņóģņØś ņ▓śļ”¼ĻĄ¼ņŚÉņä£ ņ£ĀņØśĒĢśĻ▓ī ļé«Ļ▓ī Ļ┤Ćņ░░ļÉśņŚłļŗż. ņĀæņóģ 32ņØ╝ ĒøäņŚÉļŖö VPņŚÉņä£ 98.8%ņśĆĻ│Ā, SAT+VP, EGT+VPņŚÉņä£ļŖö Ļ░üĻ░ü 98.8%, 98.7%ļĪ£ ļ░£ļ│æļÅäĻ░Ć ļåÆņĢśņ£╝ļéś, CHT+VPļŖö 87.5%ļĪ£ ļŗżļźĖ ņ▓śļ”¼ļōżĻ│╝ ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņśĆļŗż(Table 2, Fig. 1). ļ│Ė ņŗżĒŚś Ļ▓░Ļ│╝ņÖĆ ļ╣äņŖĘĒĢśĻ▓ī ĒåĀļ¦łĒåĀ Ļ░Éņłśņä▒ ĒÆłņóģ ŌĆś Jinpeng-1ŌĆÖņŚÉņä£ SA ņ▓śļ”¼Ļ░Ć TYLCV ņĀæņóģ Ēøä 10ņØ╝Ļ╣īņ¦Ć ļīĆņĪ░ĻĄ¼ņÖĆ ļ╣äĻĄÉĒĢśņŚ¼ ņ▓┤ļé┤ ļ░öņØ┤ļ¤¼ņŖż ĒĢ©ļ¤ēņØä ņ£ĀņØśĒĢśĻ▓ī Ļ░Éņåīņŗ£ņ╝░ļŖöļŹ░, ņØ┤ļŖö 2 mM ļåŹļÅäņØś SA ņ▓śļ”¼Ļ░Ć ņ▓┤ļé┤ ĒÖ£ņä▒ņé░ņåīņóģ(reactive oxygen species) ņāØņä▒ņØä ņ¢ĄņĀ£ĒĢśĻ│Ā ļ│æ ņĀĆĒĢŁņä▒ Ļ┤ĆļĀ© ĒÜ©ņåīļź╝ ņĪ░ņĀłĒĢ©ņ£╝ļĪ£ņŹ© TYLCVņŚÉ ļīĆĒĢ£ ņĀĆĒĢŁņä▒ņØä ņ”ØļīĆņŗ£ņ╝░ĻĖ░ ļĢīļ¼Ėņ£╝ļĪ£ ĒÖĢņØĖļÉśņŚłļŗż(Li ļō▒, 2019). EG ņ▓śļ”¼ļŖö NOņÖĆ SAņØś ĒĢ©ļ¤ēņØä ņČĢņĀüĒĢśņŚ¼ TYLCVņŚÉ ļīĆĒĢ£ ņĀĆĒĢŁņä▒ņØä Ē¢źņāüņŗ£Ēé©ļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ļŗż(Sun ļō▒, 2016; WangĻ│╝ Fan, 2014). Tsai ļō▒(2019)ņŚÉņä£ļŖö 200 ╬╝ g/ml EG ņĀäņ▓śļ”¼Ļ░Ć Tomato leaf curl New Delhi virus DNA AņÖĆ ļ▓ĀĒāĆņ£äņä▒ DNA (DNA B)ņØś ņČĢņĀü ņåŹļÅäļź╝ Ļ░Éņåīņŗ£ņ╝░ņ£╝ļéś, ņĀæņóģ 15ņØ╝ ĒøäņŚÉļŖö DNA BņØś ļåŹļÅäĻ░Ć ļīĆņĪ░ĻĄ¼ņÖĆ ļ╣äņŖĘĒĢ£ ņłśņżĆņ£╝ļĪ£ ņ”ØĻ░ĆĒ¢łļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż.
Fig.┬Ā1.
Effect of foliar treatments for Tomato yellow leaf curl virus (TYLCV) control in susceptible tomato cultivar ŌĆśSuperdotaerangŌĆÖ evaluated at 12, 18, and 32 days post inoculated (dpi) with TYLCV. CP, healthy control plants; VP, virus infected control plants; SAT, 2 mM salicylic acid; CHT, 0.1% chitosan; EGT, 200 ╬╝g/ml eugenol.

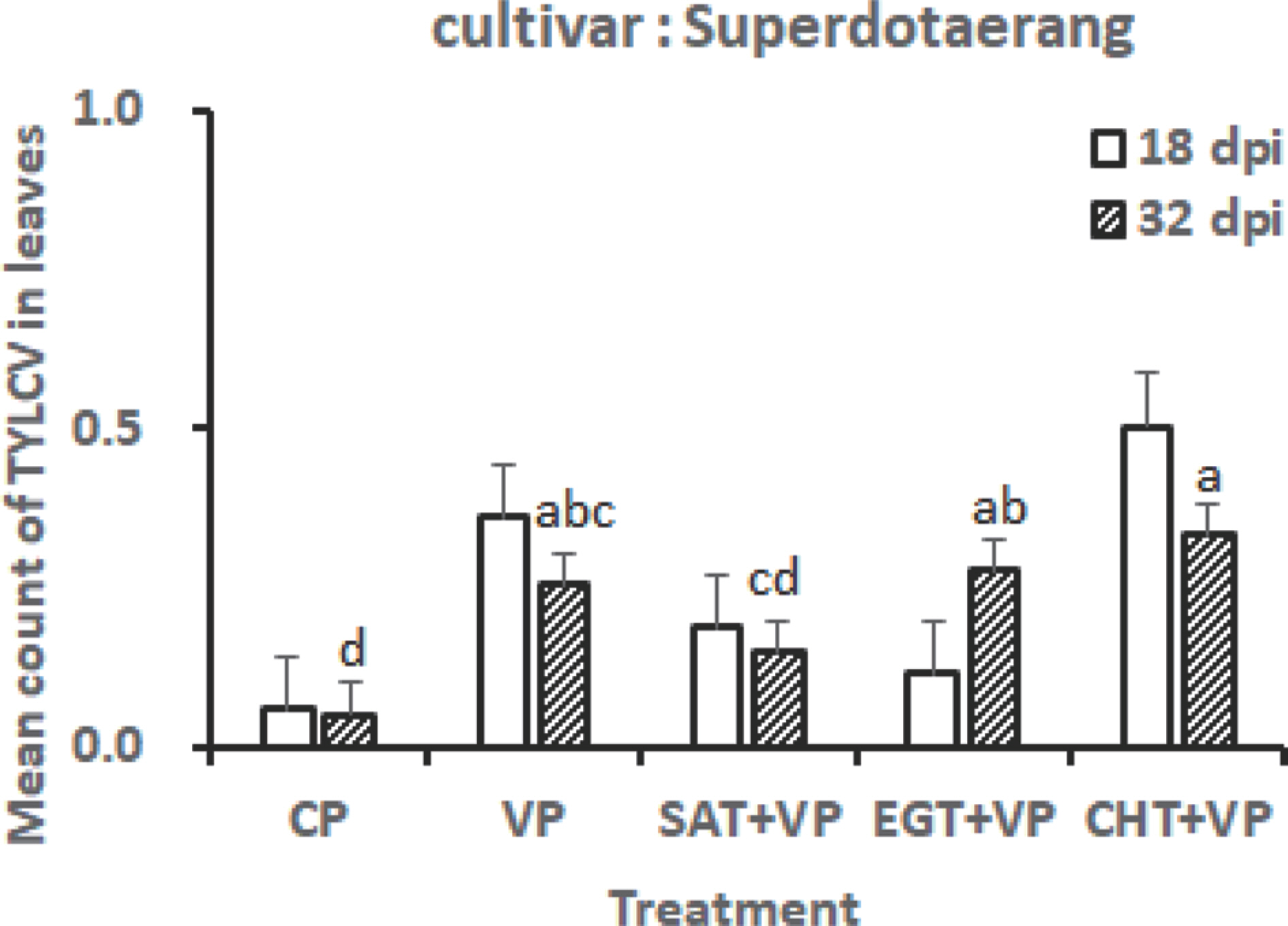
DAS-ELISA Ļ▓░Ļ│╝ļź╝ ļ╣äĻĄÉĒĢ┤ ļ│┤ļ®┤, ņĀæņóģ 18ņØ╝ Ēøä ļ░£ļ│æļÅäļŖö VPņŚÉ ļ╣äĒĢ┤ ĒĢŁļ░öņØ┤ļ¤¼ņŖż 3ņóģ ņ▓śļ”¼ĻĄ¼ņŚÉņä£ ļ░£ļ│æļÅäĻ░Ć ņ£ĀņØśĒĢśĻ▓ī ļé«Ļ▓ī ļéśĒāĆļé¼Ļ│Ā TYLCV ļåŹļÅäļŖö SAT+VPņØś ODĻ░ÆņØ┤ 0.2ļĪ£ Ļ░Ćņן ļé«ņĢśņ£╝ļéś ņ▓śļ”¼Ļ░ä ņ£ĀņØśņ░©ļŖö ņØĖņĀĢļÉśņ¦Ć ņĢŖņĢśļŗż. ņĀæņóģ 32ņØ╝ Ēøä CHT+VPņŚÉņä£ ļ░£ļ│æļÅäĻ░Ć 87.50%ļĪ£ ļŗżļźĖ ņ▓śļ”¼ĻĄ¼ņŚÉ ļ╣äĒĢ┤ ļé«Ļ▓ī ļéśĒāĆļé¼ņ£╝ļéś, TYLCV ļåŹļÅäļŖö ODĻ░ÆņØ┤ 0.3ņ£╝ļĪ£ ņśżĒ׳ļĀż Ļ░Ćņן ļåÆĻ▓ī ļéśĒāĆļé¼ļŗż(Table 2, Fig. 2). ļö░ļØ╝ņä£, ļ│Ė ņŚ░ĻĄ¼ņØś Ļ▓░Ļ│╝ņÖĆ Lapidot ļō▒(1997)ņØś Ļ▓░Ļ│╝ļĪ£ ļ»ĖļŻ©ņ¢┤ ļ│┤ņĢä ņŗØļ¼╝ņ▓┤ņØś ļ░öņØ┤ļ¤¼ņŖż ļåŹļÅäĻ░Ć ļ░£ļ│æļÅäņÖĆ ņ¢ĖņĀ£ļéś ņØ╝ņ╣śĒĢśļŖö Ļ▓āņØĆ ņĢäļŗłļØ╝ļŖö Ļ▓āņØä ĒÖĢņØĖĒ¢łņ£╝ļ®░, Ļ░ÉņŚ╝ Ēøä ļ░öņØ┤ļ¤¼ņŖż ļ│æņ¦ĢņØś ņĀĢļÅäņŚÉ ļö░ļØ╝ ņ▓┤ļé┤ ļ░öņØ┤ļ¤¼ņŖż ņ”ØņŗØļåŹļÅäņŚÉ ļ│ĆĒÖöĻ░Ć ņ׳ņØä Ļ▓āņ£╝ļĪ£ ņČöņĀĢļÉśņŚłļŗż.
Fig.┬Ā2.
Virus concentrations in tomato plants as determined by double antibody sandwich enzyme linked immunosorbent assay 18 and 32 days after Tomato yellow leaf curl virus (TYLCV) inoculation and foliar antiviral compounds spray. Values are mean┬▒standard deviation of five replicates. CP, healthy control plants; VP, virus infected control plants; SAT, 2 mM salicylic acid; EGT, 200 ╬╝g/ml eu-genol; CHT, 0.1% chitosan; dpi, days post inoculation.
ņŗ£ņäżĒåĀļ¦łĒåĀ ņ×¼ļ░░ņ¦ĆņŚÉņä£ TYLCV Ļ░ÉņŚ╝ņ¢ĄņĀ£ ĒÜ©Ļ│╝ Ļ▓ĆņĀĢ. ĒĢŁļ░öņØ┤ļ¤¼ņŖżņĀ£ 3ņóģ ņ▓śļ”¼ņŚÉ ļö░ļźĖ ĒåĀļ¦łĒåĀ TYLCV Ļ░ÉņŚ╝ļźĀĻ│╝ ņłśĒÖĢļ¤ēņØä ļ╣äĻĄÉĒĢ┤ ļ│┤ļ®┤, ĒåĀļ¦łĒåĀ ņĀĢņŗØ Ēøä 30ņØ╝ņ¦ĖņØĖ ņĀ£ 1ĒÖöļ░® ņ░®Ļ│╝ ļ╣äļīĆĻĖ░ņŚÉ TYLCV Ļ░ÉņŚ╝ļźĀņØĆ NT 1.2%, SAT 0.8%, CHT 0.8%, EGT 0.5% ņł£ņ£╝ļĪ£ ļé«ņĢśĻ│Ā, 1ĒÖöļ░® ļłäņĀü ņłśĒÖĢļ¤ēņØĆ NT 963 kg/10a, CHT 1,079 kg/10a, SAT 1,102 kg/10a, EGT 1,116 kg/10a ņł£ņ£╝ļĪ£ ļ¦ÄņĢśņ£╝ļéś ņ▓śļ”¼ Ļ░ä ņ░©ņØ┤ļŖö ņŚåņŚłļŗż. ņĀ£ 3ĒÖöļ░® ņłśĒÖĢĻĖ░ņŚÉļŖö CHT 100.0%, SAT 100.0%, EGT 98.3%, NT 96.7% ņł£ņ£╝ļĪ£ ļé«Ļ▓ī ļéśĒāĆļé¼ņ£╝ļ®░, 1ĒÖöļ░®ņŚÉņä£ 5ĒÖöļ░®Ļ╣īņ¦Ć ņ▓śļ”¼ļ│ä ņĀäņ▓┤ ņłśĒÖĢļ¤ēņØĆ SAT 3,460 kg/10a, CHT 3,640 kg/10a, NT 4,235 kg/10a, EGT 4,305 kg/10a ņł£ņ£╝ļĪ£ ļ¦ÄņĢśņ£╝ļéś ĒåĄĻ│äņĀüņ£╝ļĪ£ ņ£ĀņØśņ░©Ļ░Ć ņØĖņĀĢļÉśņ¦Ć ņĢŖņĢśļŗż(Table 3). Abd El-GawadņÖĆ Bondok (2015)ņŚÉ ļ│┤Ļ│ĀņŚÉ ņØśĒĢśļ®┤ 2 mM SAņÖĆ 0.1% CHņØś Ēś╝ĒĢ®ņ▓śļ”¼Ļ░Ć TMV Ļ░ÉņŚ╝ņØä ņ¢ĄņĀ£ĒĢśĻ│Ā ļŗ©ļÅģņ▓śļ”¼ņŚÉ ļ╣äĒĢ┤ ĒåĀļ¦łĒåĀ ņłśļ¤ēņØä ņ”ØĻ░Ćņŗ£ĒéżļŖö ĒÜ©Ļ│╝Ļ░Ć ņ׳ņŚłĻ│Ā, CHĻ│╝ Pseudomonas sp. Ēś╝ĒĢ®ņ▓śļ”¼Ļ░Ć ToLCV ļ░£ļ│æļÅäļź╝ Ļ░Éņåīņŗ£Ēé¼ ļ┐É ņĢäļŗłļØ╝ ņŗØļ¼╝ ņä▒ņןņØä ņ┤ēņ¦äĒĢśĻ│Ā ĒåĀļ¦łĒåĀņØś ņŻ╝ļŗ╣ ņłśļ¤ēņØä ņ”ØĻ░Ćņŗ£ĒéżļŖö ļō▒ ļ»ĖņāØļ¼╝Ļ│╝ ņŗØļ¼╝ ļ│æ ņĀĆĒĢŁņä▒ ņ£ĀļÅäļ¼╝ņ¦łņØś ņĪ░ĒĢ®ņ▓śļ”¼ņŚÉ ļö░ļźĖ ņāüņŖ╣ ĒÜ©Ļ│╝Ļ░Ć ļ│┤Ļ│ĀļÉ£ ļ░ö ņ׳ņ¢┤(Mishra ļō▒, 2014), ĒĢŁļ░öņØ┤ļ¤¼ņŖż ĒÜ©Ļ│╝Ļ░Ć ņØĖņĀĢļÉśļŖö ļ¼╝ņ¦łļōżņØś ņĪ░ĒĢ®ņŚÉ ļīĆĒĢ┤ņä£ļÅä ņČöĻ░Ć ņŚ░ĻĄ¼Ļ░Ć ĒĢäņÜöĒĢĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
Table┬Ā3.
The effect of antiviral compounds on TYLCV infection rates and yield of greenhouse-grown tomato
| Materialsa | Infection rate (%) | Yield per plant (kg/plant) | Early yield (kg/10a) | Total yield (kg/10a) | |
|---|---|---|---|---|---|
| 30 DAT | 50 DAT | ||||
| NT | 3/260 (1.2) | 58/60 (96.7) | 2.1 | 963 | 4,235 |
| SAT | 2/250 (0.8) | 60/60 (100.0) | 1.7 | 1,102 | 3,460 |
| CHT | 2/250 (0.8) | 60/60 (100.0) | 1.8 | 1,079 | 3,640 |
| EGT | 1/210 (0.5) | 59/60 (98.3) | 2.1 | 1,116 | 4,305 |
ņĄ£ĻĘ╝ ņŚ░ĻĄ¼ņŚÉ ļö░ļź┤ļ®┤ TYLCV ņ”ØņāüņØĆ ļ┤ä ņ×æĒśĢņŚÉ ļ╣äĒĢ┤ Ļ▓©ņÜĖ ņ×æĒśĢņŚÉ Ļ▓Įļ»ĖĒĢśĻ▓ī ļéśĒāĆļéśļ®░(Rashid ļō▒, 2008; Singh ļō▒, 2015), ņś©ļÅä ņāüņŖ╣ņŚÉ ļö░ļØ╝ TYLCV ļ░£ņāØļźĀņØ┤ ņ”ØĻ░ĆĒĢśļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłļŗż(Iftikhar ļō▒, 2021). ņØ┤ļŖö ĻČüĻĘ╣ņĀüņ£╝ļĪ£ Ļ│Āņś©ņ£╝ļĪ£ ņØĖĒĢ┤ ļ¦żĻ░£ņČ®ņØĖ ļŗ┤ļ░░Ļ░ĆļŻ©ņØ┤ ļ░£ņāØ ņ”ØĻ░ĆņŚÉ ĻĖ░ņØĖĒĢ£ Ļ▓āņ£╝ļĪ£ ļČäņäØļÉśņŚłļŗż(Zeshan ļō▒, 2016). ļö░ļØ╝ņä£ ļ│Ė ņŚ░ĻĄ¼ Ļ▓░Ļ│╝, ņāØņ£Īņ┤łĻĖ░ TYLCV Ļ░ÉņŚ╝ņłśņżĆņØ┤ 0.5-1.2%ņśĆņ£╝ļéś ņłśĒÖĢĻĖ░ņŚÉ ņĀæņ¢┤ļōżļ®┤ņä£ Ļ░ÉņŚ╝ļźĀņØ┤ 96.7-100.0%ļĪ£ ĻĖēņ”ØĒĢśņśĆļŹś Ļ▓āņØĆ ļŗ┤ļ░░Ļ░ĆļŻ©ņØ┤ņØś ļ░ĆļÅäĻ░Ć ļåÆņØĆ ņŚ¼ļ”äņ×¼ļ░░ ņ×æĒśĢņŚÉ ļ│Ė ņŚ░ĻĄ¼Ļ░Ć ņłśĒ¢ēļÉśņŚłĻĖ░ ļĢīļ¼Ėņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż. ņŗżĒŚśņŚÉ ņé¼ņÜ®ļÉ£ ĒĢŁļ░öņØ┤ļ¤¼ņŖż 3ņóģņØś ĒÜ©Ļ│╝Ļ░Ć Ļ░ÉņŚ╝ņ┤łĻĖ░ņŚÉļ¦ī ņØ╝ļČĆ ņØĖņĀĢļÉśņŚłļŹś ņØ┤ņĀä ņŚ░ĻĄ¼Ļ▓░Ļ│╝ļĪ£ ļ»ĖļŻ©ņ¢┤ ļ│╝ ļĢī, ņĀä ņāØņ£ĪĻĖ░Ļ░ä ļÅÖņĢł ļ░öņØ┤ļ¤¼ņŖżņØś Ļ░ÉņŚ╝ņ£äĒŚśņŚÉ ļģĖņČ£ļÉśņ¢┤ņ׳ļŖö ĒåĀļ¦łĒåĀ ņ×¼ļ░░ĒśäņןņŚÉņä£ļŖö ņĢäņ¦ü ņĀüņÜ®ĒĢśĻĖ░ļŖö ņ¢┤ļĀżņÜĖ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
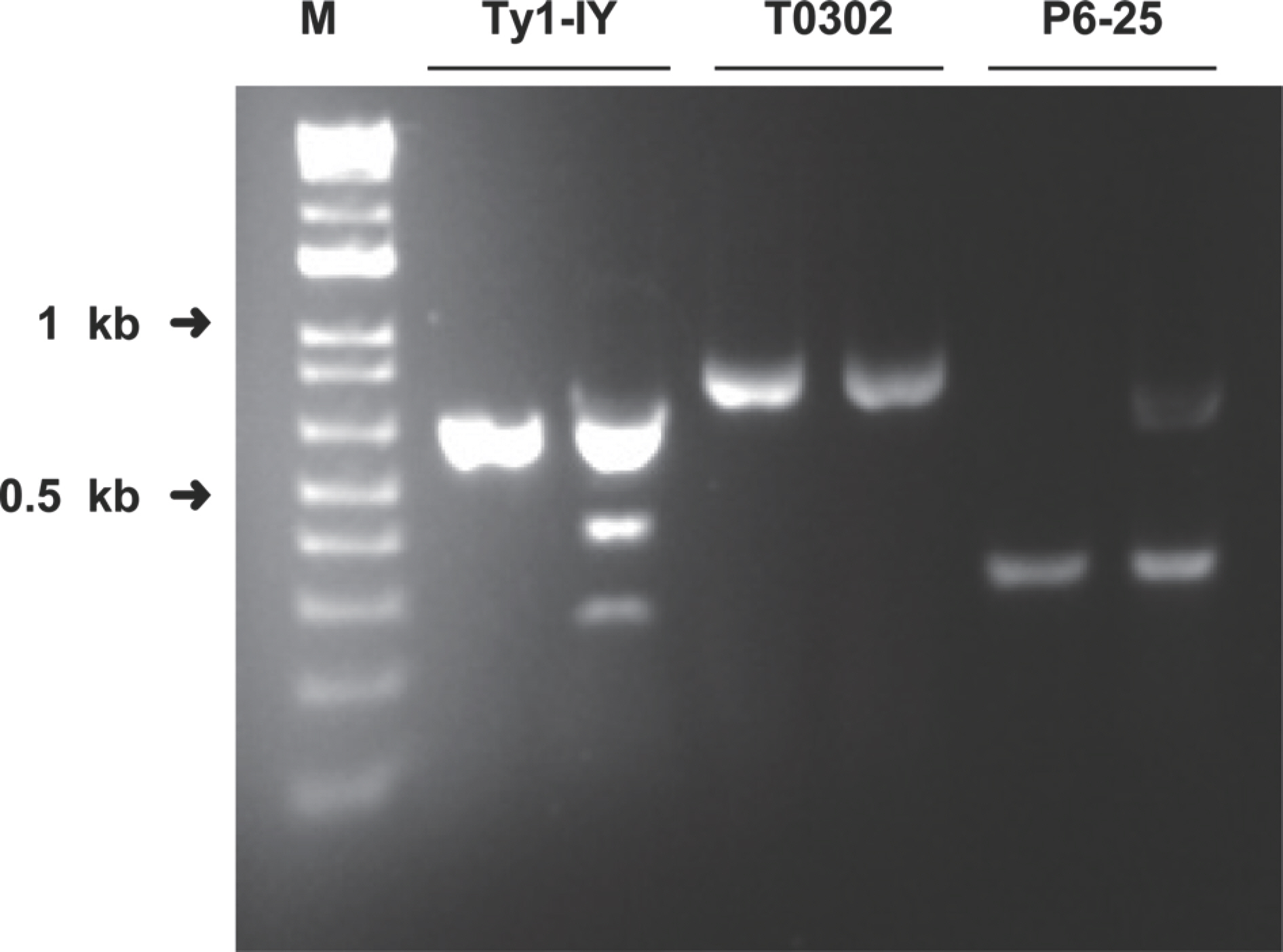
ĒåĀļ¦łĒåĀ ņŗ£ĒŚśĒÆłņóģņØś TYLCV ļé┤ļ│æņä▒ĒÅēĻ░Ć. ņŗ£ĒŚśĒÆłņóģ ŌĆśņŖłĒŹ╝ļÅäĒā£ļ×æŌĆÖņŚÉņä£ļŖö ļé┤ņä▒ ņ£ĀņĀäņ×É ļ¦łņ╗żĻ░Ć ļ░£Ļ▓¼ļÉśņ¦Ć ņĢŖņĢśņ£╝ļ®░, ļ░£ļ│æļźĀļÅä 94.4%ļĪ£ ļåÆņĢśļŗż. ļ░śļ®┤, TYLCV ļé┤ļ│æņä▒ņ£╝ļĪ£ ņĢīļĀżņ¦ä ļīĆļ╣äĒÆłņóģ ŌĆś TY ņ×ÉņØ┤ņ¢ĖņĖĀŌĆÖļŖö Ty1/3 ņ£ĀņĀäņ×ÉņóīņŚÉņä£ņØś ņØ┤ĒśĢņĀæĒĢ®ņØ┤ ļ░£Ļ▓¼ļÉśņŚłĻ│Ā Ty-3a ņ£ĀņĀäņ×É ņĪ┤ņ×¼Ļ░Ć ĒÖĢņØĖļÉśņŚłņ£╝ļ®░, ļ░£ļ│æļźĀņØ┤ 0.0%ļĪ£ ļ¦żņÜ░ ļé«ņĢśļŗż(Table 4, Fig. 3). Verlaan ļō▒(2013)ņŚÉņä£ TYLCVņŚÉ ļīĆĒĢ£ ļé┤ņä▒ ņ£ĀņĀäņ×É Ty-1Ļ│╝ Ty-3 ļśÉļŖö Ty-3aĻ░Ć 6ļ▓ł ņŚ╝ņāēņ▓┤ņŚÉ ņĪ┤ņ×¼ĒĢśļ®░, ļæÉ ņ£ĀņĀäņ×ÉĻ░Ć ļÅÖņØ╝ĒĢ£ ņ£ĀņĀäņ×ÉņóīņØś ļīĆļ”Įņ£ĀņĀäņ×Éņ×äņØ┤ ņ×ģņ”ØļÉ©ņŚÉ ļö░ļØ╝ ŌĆś TYņ×ÉņØ┤ņ¢ĖņĖĀŌĆÖ ĒÆłņóģņØś Ty-1Ļ│╝ Ty-3 ņ£ĀņĀäņ×ÉļŖö ļČĆļ¬© ņżæ ĒĢ£ņ¬Įņ£╝ļĪ£ļČĆĒä░ ņ£ĀļלļÉśņŚłņØä Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż. ļśÉĒĢ£ Ty-1 ļé┤ņä▒ņØä ļŗ┤ļŗ╣ĒĢśļŖö ņ£ĀņĀäņ×ÉĻ░Ć DFDGD-class RNA-dependent RNA polymeraseļĪ£ ĒÖĢņØĖļÉśņŚłĻ│Ā, TYLCVņØś DNA ļ│ĄņĀ£ ļ░Å ļ®öĒŗĖĒÖöņŚÉ ņśüĒ¢źņØä ļ»Ėņ╣śļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłļŗż(Butterbach ļō▒, 2014). ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ĒÖ£ņÜ®ĒĢ£ Ty1/3 ņ£ĀņĀäņ×ÉņóīņŚÉ ļīĆĒĢ£ CAPS ļ¦łņ╗żļŖö Ty-1Ļ│╝ Ty-3 ļśÉļŖö Ty-3a ļé┤ņä▒ ņ£ĀņĀäņ×Éļź╝ ĒżĒĢ©ĒĢśĻ│Ā ņ׳ņ£╝ļ®░ ņØ┤ ņ£ĀņĀäņ×Éļōżļź╝ ļ│┤ņ£ĀĒĢ£ ļŗżņłśņØś ņ£Āļ¤ĮĒÆłņóģņŚÉņä£ TYLCV ļ░£ļ│æļźĀņØ┤ 3.3% ņØ┤ĒĢśļĪ£ ļ¦żņÜ░ ļé«Ļ▓ī ļéśĒāĆļé¼ļŗż(Kim ļō▒, 2013).
Fig.┬Ā3.
Amplified fragment patterns of the cleaved amplified polymorphic sequence marker Ty1-SspI (A), sequence characterized amplified region marker Ty2 T0302 (B), and Ty3 P6-25 (C) in two tomato cultivars. M, 1 kb DNA ladder; lane 1, Superdotaerang; 2, TY Giants.
Table┬Ā4.
The disease resistance assay of TYLCV in pot seedling on tomato cultivars used in this study
| Cultivar | Company | Marker genotypea | Disease severity (%) | ELISA | ||
|---|---|---|---|---|---|---|
| Ty1/3 | Ty-2 | Ty-3 | ||||
| Superdotaerang | Coregon | S | S | S | 94.4 a | 0.2 a |
| TY Giants | Mifko | H | S | H | 0.0 b | 0.1 b |
ļö░ļØ╝ņä£, ļ│Ė ņŚ░ĻĄ¼ņŚÉ ĒÖ£ņÜ®ĒĢ£ CAPS ļ¦łņ╗żļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ TYLCV ļé┤ņä▒ ņ£ĀņĀäņ×É ļ│┤ņ£Ā ņŚ¼ļČĆļź╝ ĒÖĢņØĖĒĢ£ ĒøäņŚÉ ĒÆłņóģņØä ņäĀĒāØĒĢśļŖö Ļ▓āņØ┤ ļ░öņØ┤ļ¤¼ņŖżļ│æņØś ļīĆļ░£ņāØņØä ņśłļ░®ĒĢśĻ│Ā, ĒåĀļ¦łĒåĀņØś ņĢłņĀĢņāØņé░ņŚÉ ļÅäņøĆņØ┤ ļÉĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print