|
 |
| Res. Plant Dis > Volume 26(3); 2020 > Article |
|
ABSTRACT
Powdery mildew is a common and serious disease of the Cucurbitaceae including cucumber (Cucumis sativus) in most areas of the world. To identify causal agents of the powdery mildew and their physiological race(s), we collected cucumber leaves displaying typical symptoms of powdery mildew from different locations in Korea. Based on morphological and molecular characteristics, all powdery mildew isolates were identified as an obligate biotrophic fungal pathogen, Podosphaera xanthii. After inoculation at melon (Cucumis melo) differentials to identify the fungal race(s), P. xanthii isolate MI180427 and IC190611 were identified as race 1 which has been repeatedly reported as dominant race in Korea. However, another isolate SE180328 produced different disease response in the tested differentials, being identified as race 2 which has not been reported in Korea. To confirm the race of SE180328, we inoculated additional melon differentials and determined the isolate as race 2F that is the prevalent race of powdery mildew in Beijing, China. Report of this new race 2F in Korea will be helpful for future breeding programs to develop resistant varieties to this race.
ĒØ░Ļ░ĆļŻ©ļ│æ(Powdery mildew)ņØĆ ņśżņØ┤(Cucumis sativus)ļź╝ ĒżĒĢ©ĒĢśļŖö ļ¬©ļōĀ ļ░ĢĻ│╝(Cucurbitaceae) ņ×æļ¼╝ņŚÉņä£ Ļ░Ćņן ņŗ¼Ļ░üĒĢ£ Ēö╝ĒĢ┤ļź╝ ņØ╝ņ£╝ĒéżļŖö ļ│æ ņżæ ĒĢśļéśņØ┤ļŗż. ņśżņØ┤ ĒØ░Ļ░ĆļŻ©ļ│æņŚÉ Ļ░ÉņŚ╝ļÉśļ®┤ ņśżņØ┤ņØś ņ×ÄĻ│╝ ņżäĻĖ░ļź╝ ņżæņŗ¼ņ£╝ļĪ£ ĒØ░ņāē ļČäļ¦É ĒśĢĒā£ņØś ĻĘĀņé¼ņ▓┤ņÖĆ ļČäņāØĒżņ×ÉĻ░Ć ņāØņä▒ļÉśĻ│Ā, ņŗ¼ĒĢśĻ▓ī Ļ░ÉņŚ╝ļÉ£ ņ×ÄņØĆ Ļ┤æĒĢ®ņä▒ņØ┤ Ļ░ÉņåīĒĢśĻ│Ā ĻĮāĻ│╝ Ļ│╝ņŗżņØś ņāØņä▒ņŚÉļÅä ņśüĒ¢źņØä ņżĆļŗż(Rabelo ļō▒, 2017). Ļ░ÉņŚ╝ ņ┤łĻĖ░ ļŗ©Ļ│äņØś ĒØ░Ļ░ĆļŻ©ļ│æņØĆ ņŗØļ¼╝ ņ×Éņ▓┤ņŚÉ ņśüĒ¢źņØä ņŻ╝ņ¢┤ ņŗØļ¼╝ņØś Ļ┤┤ņé¼ļź╝ ņØ╝ņ£╝ĒéżĻ▒░ļéś ņłśĒÖĢļ¤ēņØä Ļ░Éņåīņŗ£ĒéżļŖö ļ░śļ®┤, Ļ░ÉņŚ╝ ĒøäĻĖ░ ļŗ©Ļ│äļŖö ņØ╝ļ░śņĀüņ£╝ļĪ£ Ļ│╝ņŗżņØś ĒÆłņ¦łņØä ņĀĆĒĢśņŗ£Ēé©ļŗż(Huang ļō▒, 2000). ņśżņØ┤ņŚÉ ĒØ░Ļ░ĆļŻ©ļ│æņØä ņØ╝ņ£╝ĒéżļŖö ļīĆĒæ£ņĀüņØĖ ļ│æņøÉĻĘĀņØĆ ļæÉ Ļ░Ćņ¦ĆņØś ņĀłļīĆĻĖ░ņāØĻĘĀ(obligate parasite) Golovinomyces cichoracearum (syn. Erysiphe cichoracearum)Ļ│╝ Podosphaera xanthii (syn. Sphaerotheca fuliginea)ņØ┤ļ®░(BertrandņÖĆ Pitrat, 1989; Hosoya ļō▒, 1999), Ēśäņ×¼ ĻĄŁļé┤ņŚÉņä£ ļŖö P. xanthiiĻ░Ć ņŻ╝ļĪ£ ĒØ░Ļ░ĆļŻ©ļ│æņØä ņØ╝ņ£╝ĒéżļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņ¢┤ ņ׳ļŗż(Kim ļō▒, 2015). ņĄ£ĻĘ╝ ņŗ£ņäż ņ×¼ļ░░Ļ░Ć ņ”ØĻ░ĆĒĢśĻ│Ā ņś©ļé£ĒÖöĻ░Ć Ļ░ĆņåŹĒÖöļÉ©ņŚÉ ļö░ļØ╝ P. xanthiiņŚÉ ņØśĒĢ£ ļ│æ Ēö╝ĒĢ┤Ļ░Ć ņ”ØĻ░ĆĒĢśĻ│Ā ņ׳ļŖö ņČöņäĖņØ┤ļ®░ (Hong ļō▒, 2018; Tetteh ļō▒, 2013), ĒØ░Ļ░ĆļŻ©ļ│æ ņĀĆĒĢŁņä▒ ĒÆłņóģņØ┤ ņāłļĪŁĻ▓ī ņČ£ĒśäĒĢśļŖö raceņŚÉ ņØśĒĢ┤ ņØ┤ļ│æĒÖöļÉśļŖö ĒśäņāüņØ┤ ļ░śļ│ĄļÉśĻ│Ā ņ׳ļŗż. ļ│Ė ņŚ░ĻĄ¼ļŖö ĻĄŁļé┤ ņśżņØ┤ ĒØ░Ļ░ĆļŻ©ļ│æņØä ņØ╝ņ£╝ĒéżļŖö ņøÉņØĖĻĘĀņ£╝ļĪ£ P. xanthii isolatesņØä ļČäļ”¼ ļÅÖņĀĢĒĢśņśĆņ£╝ļ®░ ļ®£ļĪĀ ĒīÉļ│ä ņŗØļ¼╝ņØä ņØ┤ņÜ®ĒĢśņŚ¼ race 1ņÖĆ race 2ļĪ£ ĒīÉļ│äĒĢśņśĆļŗż. ļśÉĒĢ£, ĻĄŁļé┤ņŚÉņä£ ņāłļĪŁĻ▓ī ļ░£Ļ▓¼ļÉ£ race 2ņØś Ļ▓ĮņÜ░ ņČöĻ░ĆņĀüņØĖ ļ®£ļĪĀ ĒīÉļ│ä ĻĖ░ņŻ╝ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņĄ£ņóģņĀüņ£╝ļĪ£ race 2FļĪ£ Ļ▓░ņĀĢĒĢśņśĆļŗż.
ĻĄŁļé┤ņŚÉņä£ ļ░£ņāØĒĢśĻ│Ā ņ׳ļŖö ņśżņØ┤ ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀ ņĪ░ņé¼ļź╝ ņ£äĒĢśņŚ¼ Ļ▓ĮĻĖ░ļÅä Ļ┤æņŻ╝(Gwangju), Ļ▓ĮĻĖ░ļÅä ņØ┤ņ▓£(Icheon), ņĀäļØ╝ļČüļÅä Ļ╣ĆņĀ£(Gimje), ņä£ņÜĖĒŖ╣ļ│äņŗ£(Seoul), Ļ▓Įņāüļé©ļÅä ļ░Ćņ¢æ(Miryang) ņ¦ĆņŚŁņØś ņ×¼ļ░░ļåŹĻ░ĆņŚÉņä£ ĒØ░Ļ░ĆļŻ©ļ│æņØ┤ ļ░£ņāØĒĢ£ ņśżņØ┤ ņ×ÄņØä ņ▒äņ¦æĒĢśņśĆļŗż(Fig. 1A, B). ņ▒äņ¦æĒĢ£ ņ×ÄņŚÉ ĒśĢņä▒ļÉ£ ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀņØś ĻĘĀņŻ╝ļź╝ ļÅÖņĀĢĒĢśĻĖ░ ņ£äĒĢ┤ ņØ┤ļōżņØä ņØ┤ļ│æņä▒ņØĖ ņĪ░ņØĆļ░▒ļŗżļŗżĻĖ░ņśżņØ┤(FarmHannong, Seoul, Korea)ņØś ļ¢Īņ×Ä Ēś╣ņØĆ ļ│Ėņ×ÄņŚÉ ņ”ØņŗØĒĢśļŖö ļ░®ļ▓Ģ(Lee ļō▒, 2004)ņ£╝ļĪ£ ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀņØä ņł£ņłś ļČäļ”¼ĒĢśņśĆļŗż.
ņśżņØ┤ņÖĆ ļ®£ļĪĀņØĆ ņóģņ×É ņåīļÅģ Ēøä ļ®ĖĻĘĀļÉ£ ņ”ØļźśņłśņŚÉņä£ ļ░£ņĢäļź╝ ņ£ĀļÅäĒĢśņśĆĻ│Ā ļŗżĻ│Ą ĒöīļØ╝ņŖżĒŗ▒ ĒżĒŖĖņŚÉ ņøÉņśłņÜ®ņāüĒåĀ 2ĒśĖ(Seoul Bio, Gwangmyeong, Korea)ļź╝ ļäŻĻ│Ā ļ░£ņĢäļÉ£ ņóģņ×Éļź╝ ĒżĒŖĖļŗ╣ 1ļ”Įņö® ņŗ¼ņ¢┤ņŻ╝ņŚłļŗż. ļ¬©ļōĀ ņŗØļ¼╝ņØĆ 23┬░ 16ņŗ£Ļ░ä Ļ┤æņĪ░Ļ▒┤, 8ņŗ£Ļ░ä ņĢöņĪ░Ļ▒┤ņØ┤ ņ£Āņ¦ĆļÉśļŖö ņŗØļ¼╝ ņāØņןņāü Ēś╣ņØĆ ņäĖņóģļīĆĒĢÖĻĄÉ ņ║ĀĒŹ╝ņŖżņŚÉ ņ׳ļŖö ņ£Āļ”¼ņś©ņŗżņŚÉņä£ ņ×¼ļ░░ĒĢśņśĆļŗż. ņśżņØ┤ ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀņØś ņł£ņłś ļČäļ”¼ņÖĆ ĒÜ©Ļ│╝ņĀüņØĖ ņ”ØņŗØņØä ņ£äĒĢśņŚ¼ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņ×Ä ņĀłĒÄĖ(leaf disk)ņØä ņØ┤ņÜ®ĒĢ£ ļ░®ļ▓Ģ(Fanourakis, 1991; Lee ļō▒, 2004)ņØä ņØ╝ļČĆ ļ│ĆĒśĢĒĢśņŚ¼, Ļ░ÉņŚ╝ņ×Ä ņĀłĒÄĖņØä Ļ▒┤ņĀäņ×Ä Ēś╣ņØĆ Ļ▒┤ņĀäņ×Ä ņĀłĒÄĖĻ│╝ ņĀæņ┤ēņŗ£ņ╝£ ņĀæņóģņØä ņ£ĀļÅäĒĢśļŖö ŌĆśdisk-to-diskŌĆÖ ļ░®ļ▓ĢņØä ņé¼ņÜ®ĒĢśņśĆļŗż. Ļ▒┤ņĀäņ×Ä Ēś╣ņØĆ Ļ▒┤ņĀäņ×Ä ņĀłĒÄĖ(1.5├Ś1.5 cm)ņØä 70% ņŚÉĒāäņś¼ļĪ£ ņåīļÅģĒĢśĻ│Ā, ļ░░ņ¦Ć(25 mg/ml benzimidazol, 1% phytoagar) (Gafni ļō▒, 2015)Ļ░Ć ļČäņŻ╝ļÉ£ ĒÄśĒŖĖļ”¼ļööņē¼ņŚÉ ņ╣śņāüĒĢ£ Ēøä ņ×¼ļ░░ ļåŹĻ░ĆņŚÉņä£ ņ▒äņ¦æĒĢ£ ĒØ░Ļ░ĆļŻ©ļ│æ Ļ░ÉņŚ╝ņ×ÄņØś ņĀłĒÄĖ(0.8├Ś0.8 cm)ņØä Ļ▒┤ņĀäņ×Ä Ēś╣ņØĆ Ļ▒┤ņĀäņ×Ä ņĀłĒÄĖ ņ£äņŚÉ ņś¼ļĀżņŻ╝Ļ│Ā ļ░Ćļ┤ēĒĢśņśĆļŗż. ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀņØĆ ļ░Ćļ┤ēļÉ£ ĒÄśĒŖĖļ”¼ļööņē¼ņŚÉņä£ 23┬░, 24ņŗ£Ļ░ä Ļ┤æņĪ░Ļ▒┤ņ£╝ļĪ£ ņĢĮ 10ņØ╝Ļ░ä ņ”ØņŗØĒĢśĻ│Ā, ņØ┤ņāüņØś ņ”ØņŗØņØä ņĄ£ņåī 3ĒÜī ņØ┤ņāü ļ░śļ│ĄĒĢśņŚ¼ ņł£ņłś ļČäļ”¼ĒĢśņśĆļŗż. Ļ▓ĮĻĖ░ļÅä Ļ┤æņŻ╝, Ļ▓ĮĻĖ░ļÅä ņØ┤ņ▓£, ņĀäļØ╝ļČüļÅä Ļ╣ĆņĀ£,ņä£ņÜĖĒŖ╣ļ│äņŗ£, Ļ▓Įņāüļé©ļÅä ļ░Ćņ¢æņŚÉņä£ ņłśņ¦æļÉ£ ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀņØś ļČäļ”¼ ĻĘĀņŻ╝ļź╝ Ļ░üĻ░ü GW170710, IC190611, KI170723, SE180328, MI180427ļØ╝Ļ│Ā ļ¬ģļ¬ģĒĢśņśĆļŗż.
ļČäļ”¼ ĻĘĀņŻ╝ļōżņØś ĒśĢĒā£ņĀü ļČäņäØņØä ņ£äĒĢśņŚ¼ ņ”ØņŗØļÉ£ ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀņØś ĻĘĀņé¼ņ▓┤ļź╝ ļ®ĖĻĘĀļÉ£ Ēīüņ£╝ļĪ£ ĻĖüņ¢┤ļé┤ņ¢┤ ļ®ĖĻĘĀ ņ”Øļźśņłś 200 ╬╝lļĪ£ ĒؼņäØĒĢśĻ│Ā Ļ┤æĒĢÖĒśäļ»ĖĻ▓Į(Eclipse Ti, Nikon, Tokyo, Japan)ņŚÉņä£ Ļ┤Ćņ░░ĒĢśņśĆļŗż. ĻĄŁļé┤ņŚÉņä£ ņ▒äņ¦æĒĢ£ ņśżņØ┤ ĒØ░Ļ░ĆļŻ©ļ│æņØś 5Ļ░Ćņ¦Ć ļČäļ”¼ ĻĘĀņŻ╝ļōżņØś(KI170723, GW170710, SE180328, MI180427 ļ░Å IC190611) Ēżņ×ÉļōżņØĆ ļ¼┤ņāē ĒāĆņøÉĒśĢņØś ĒśĢĒā£ĒĢÖņĀü ĒŖ╣ņ¦ĢņØ┤ P. xanthiiņÖĆ ļÅÖņØ╝ĒĢśņśĆļŗż(Fig. 1C). Ļ░ü ņ¦ĆņŚŁļ│ä ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀņØś ļČäņ×ÉņāØļ¼╝ĒĢÖņĀü ĒŖ╣ņ¦ĢņØä ļ╣äĻĄÉĒĢśĻĖ░ ņ£äĒĢśņŚ¼ KI170723, GW170710, SE180328, MI180427 ļ░Å IC190611ņØś genomic DNAļź╝ cetyl trimethyl ammonium bromide (CTAB)ļ▓Ģ(Porebski ļō▒, 1997)ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņČöņČ£ĒĢśņśĆļŗż. ņäĀĒ¢ē ņŚ░ĻĄ¼(Pirondi ļō▒, 2015)ļź╝ ļö░ļØ╝ņä£ internal transcribed spacer (ITS) ņśüņŚŁņØä ITS1 (5ŌĆ▓-TCCGTAGGTGAACCTGCGG-3ŌĆ▓)Ļ│╝ ITS4 (5ŌĆ▓-TCCTCCGCTTATTGATATGC-3ŌĆ▓)ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņżæĒĢ®ĒÜ©ņåīņŚ░ņćäļ░śņØæ(polymerase chain reaction)ņ£╝ļĪ£ ņ”ØĒÅŁņŗ£ņ╝░ļŗż. ņ”ØĒÅŁļÉ£ ņé░ļ¼╝ļōżņØś ņŚ╝ĻĖ░ņä£ņŚ┤ņØĆ BLAST search (https://blast.ncbi.nlm.nih.gov/Blast.cgi)ļź╝ ņØ┤ņÜ®ĒĢ£ ļ╣äĻĄÉ ļČäņäØ Ļ▓░Ļ│╝ GenBanKņŚÉ ļō▒ļĪØļÉ£ P. xanthiiņØś ITS (accession no. KJ698669.1)ņØś ņŚ╝ĻĖ░ņä£ņŚ┤Ļ│╝ 100% ņØ╝ņ╣śĒĢśņśĆļŗż(data not shown). ļö░ļØ╝ņä£, ņ▒äņ¦æļÉ£ ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀļōżņØś ļČäļ”¼ĻĘĀņŻ╝ļōżņØĆ P. xanthiiņ×äņØä ņĢī ņłś ņ׳ņŚłļŗż.
ļ│æ ņĀĆĒĢŁņä▒ ĒÆłņóģ ņ£Īņä▒ņØä ņ£äĒĢ┤ņä£ļŖö ņĀĆĒĢŁņä▒ Ļ▓ĆņĀĢņŚÉ ņé¼ņÜ®ĒĢĀ ļ│æņøÉĻĘĀņØś race ĻĘ£ļ¬ģņØ┤ ņäĀĒ¢ēļÉśņ¢┤ņĢ╝ ĒĢśļŖöļŹ░, ņśżņØ┤ņŚÉņä£ ļ░£ļ│æĒĢśļŖö P. xanthii Ļ▓ĮņÜ░ ļŗżņ¢æĒĢ£ ņāØļ”¼ĒśĢ(physiological race)ļōżņØ┤ ļ│┤Ļ│ĀļÉśņ¢┤ ņ׳ņ£╝ļéś ņĀĢļ”ĮļÉśņ¢┤ ņ׳ņ¦Ć ņĢŖņĢä ņ£ĪņóģņŚÉ ņØ┤ņÜ®ĒĢśĻĖ░ ņ¢┤ļĀĄļŗż(Lee ļō▒, 2014). ļīĆņŗĀņŚÉ P. xanthii ļŖö ļ░ĢĻ│╝ ņ×æļ¼╝ņØĖ ļ®£ļĪĀ, ņłśļ░Ģ, ņśżņØ┤ļź╝ ļ¬©ļæÉ ĻĄÉņ░©Ļ░ÉņŚ╝ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ (Cohen ļō▒, 2000) ņŻ╝ļĪ£ ļ®£ļĪĀ ĒīÉļ│ä ĒÆłņóģņØä ņØ┤ņÜ®ĒĢśņŚ¼ raceļź╝ Ļ▓░ņĀĢĒĢśĻ│Ā ņ׳ļŗż(Kuzuya ļō▒, 2006). 1935ļģä ļ»ĖĻĄŁņŚÉņä£ ņ£Īņä▒ļÉ£ ļ®£ļĪĀ ĒØ░Ļ░ĆļŻ©ļ│æ ņĀĆĒĢŁņä▒ Ļ│äĒåĄņØĖ ŌĆśPMR 45ŌĆÖņŚÉ ļ░£ļ│æĒĢśļŖö ĻĘĀņØä race 1, ŌĆśPMR 45ŌĆÖņŚÉ ļ░£ļ│æĒĢśņ¦Ć ņĢŖļŖö ĻĘĀņØä race 2ļĪ£ ļČäļźśĒĢśņśĆļŗż(Jagger ļō▒, 1938). 1946ļģä ļ»ĖĻĄŁņŚÉņä£ ņ£Īņä▒ļÉ£ race 1Ļ│╝ race 2ņŚÉ ņĀĆĒĢŁņä▒ņØä Ļ░¢ļŖö ŌĆśPMR 5ŌĆÖļź╝ ņØ┤ļ│æĒÖö ņŗ£ĒéżļŖö ĻĘĀņØä race 3ņ£╝ļĪ£ ļČäļźśĒĢśņśĆļŗż(Pryor ļō▒, 1946). ņØ┤ļź╝ ĻĖ░ļ│Ėņ£╝ļĪ£ ĒĢśņŚ¼ P. xanthiiņØś race ĒīÉļ│äņØĆ ņØ╝ļ░śņĀüņ£╝ļĪ£ 4Ļ░Ćņ¦Ć ļ®£ļĪĀ ĒÆłņóģ(ŌĆśTopmarkŌĆÖ, ŌĆśPMR 45ŌĆÖ, ŌĆśPMR 6ŌĆÖ ļ░Å ŌĆśMR-1ŌĆÖ)ņØä ņØ┤ņÜ®ĒĢśņŚ¼ race 1, 2, 3ņ£╝ļĪ£ ĒīÉļ│äĒĢśĻ│Ā ņ׳ļŗż(Zitter et al., 1996) (Table 1). ļ│Ė ņŚ░ĻĄ¼ņØś race ĒīÉļ│äņØä ņ£äĒĢ┤ņä£ļŖö ņ£äņŚÉņä£ ņäżļ¬ģĒĢ£ ļ░öņÖĆ Ļ░ÖņØ┤ ņ×Ä ņĀłĒÄĖņØä ņØ┤ņÜ®ĒĢ£ ļ░®ļ▓Ģ(Fanourakis, 1991; Lee ļō▒, 2004)ņØä ņØ╝ļČĆ ļ│ĆĒśĢĒĢ£ ŌĆśdisk-to-diskŌĆÖļ▓ĢņØä ņØ┤ņÜ®ĒĢśņśĆļŗż. ņĀæņóģ Ēøä ņĢĮ 14ņØ╝ņŚÉ ņé¼ņ¦ä ņ┤¼ņśü Ēøä ImageJ ĒöäļĪ£ĻĘĖļש(ver. 1.53c, National Institutes of Health, Bethesda, MD, USA)ņØś ŌĆ£Color thresholdŌĆØ (https://imagej.nih.gov/ij/)ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņĀĢļ¤ēĒÖöĒĢśņśĆņ£╝ļ®░ Ļ░ÉņŚ╝ņ×Ä ņĀłĒÄĖņØś Ēü¼ĻĖ░ļź╝ ĻĖ░ņżĆņ£╝ļĪ£ Ļ▒┤ņĀäņ×ÄņØś ĒØ░Ļ░ĆļŻ©ļ│æ ļ│æļ░śļ®┤ņĀüļźĀ(%)ņØä Ļ│äņé░ĒĢśņśĆļŗż. ĒÅēĻĘĀ ļ░£ļ│æ ņĀĢļÅäĻ░Ć 10% ņØ┤ĒĢśņØś Ļ▓ĮņÜ░ņŚÉļŖö ņĀĆĒĢŁņä▒(resistant, R) 11%-30%ļŖö ņżæļÅäņĀĆĒĢŁņä▒(intermediate resistant, IR), 31% ņØ┤ņāüņØĆ Ļ░Éņłśņä▒(susceptible, S)ņ£╝ļĪ£ ĒīÉņĀĢĒĢśņśĆļŗż.
ļČäļ”¼ ĻĘĀņŻ╝ MI180427ņÖĆ IC190611ņØś raceļź╝ ĻĘ£ļ¬ģĒĢśĻĖ░ ņ£äĒĢ£ ņĀæņóģ Ļ▓░Ļ│╝, MI180427ļŖö ŌĆśTopmarkŌĆÖņŚÉņä£ļŖö 51.1%ļĪ£ Ļ░Éņłśņä▒(S)ņØä ļ│┤ņśĆņ£╝ļ®░, ŌĆśPMR 45ŌĆÖņŚÉņä£ 1.6%, ŌĆśPMR 6ŌĆÖņŚÉņä£ 0.6% ĻĘĖļ”¼Ļ│Ā ŌĆśMR-1ŌĆÖņŚÉņä£ 0.3%ņØś ļ░£ļ│æ ņĀĢļÅäļĪ£ ņĀĆĒĢŁņä▒(resistance, R)ņØä ļéśĒāĆļé┤ņŚłļŗż(Fig. 2). IC190611ļŖö ŌĆśTopmarkŌĆÖņŚÉņä£ 74.9% (S), ŌĆśPMR 45ŌĆÖņŚÉņä£ 1.1% (R), ŌĆśPMR 6ŌĆÖņŚÉņä£ 2.3% (R) ĻĘĖļ”¼Ļ│Ā ŌĆśMR-1ŌĆÖņŚÉņä£ 0.7% (R)ņØś ļ░£ļ│æ ņĀĢļÅäļź╝ ļéśĒāĆļé┤ņŚłļŗż(Fig. 3). ļö░ļØ╝ņä£, ļ░Ćņ¢æĻ│╝ ņØ┤ņ▓£ņŚÉņä£ ļČäļ”¼ĒĢ£ ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀņØĆ Zitter ļō▒(1996)ņØś race ĒīÉļ│ä ĻĖ░ņżĆņŚÉ ļö░ļØ╝ race 1ņØ┤ļØ╝ļŖö Ļ▓āņØä ņĢī ņłś ņ׳ņŚłļŗż (Table 1). P. xanthiiņØś ņŚ¼ļ¤¼ race ņżæ race 1ņØĆ ļ»ĖĻĄŁ ļÅÖļČĆņ¦ĆņŚŁņŚÉņä£ Ļ░Ćņן ĒØöĒĢśĻ▓ī ņĪ┤ņ×¼ĒĢśļŖö ņŻ╝ņÜöĒĢ£ ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀņØ┤ļ®░(Zitter et al., 1996), ĻĄŁļé┤ņŚÉņä£ļÅä ņÜ░ņĀÉĒĢśļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉ£ raceņØ┤ļŗż(Kim ļō▒, 2016; Lee ļō▒, 2014).
ļČäļ”¼ ĻĘĀņŻ╝ SE180328ņØś ņĀĆĒĢŁņä▒ Ļ▓ĆņĀĢ Ļ▓░Ļ│╝, ŌĆśTopmarkŌĆÖņŚÉņä£ 68.2% (S), ŌĆśPMR 45ŌĆÖņŚÉņä£ 31.0% (S), ŌĆśPMR 6ŌĆÖņŚÉņä£ 1.7% (R) ĻĘĖļ”¼Ļ│Ā ŌĆśMR-1ŌĆÖņŚÉņä£ 6.9% (R)ņØś ļ░£ļ│æ ņĀĢļÅäļź╝ ļéśĒāĆļé┤ņŚłļŗż(Fig. 4). ņÜ░ļ”¼ļŖö ļ│Ė Ļ▓ĆņĀĢ Ļ▓░Ļ│╝ļź╝ ĻĖ░ņĪ┤ņŚÉ ļ│┤Ļ│ĀļÉśņŚłļŹś ņŚ░ĻĄ¼ Ļ▓░Ļ│╝(Lee ļō▒, 2014; Zitter ļō▒, 1996)ņÖĆ ļ╣äĻĄÉĒĢśņŚ¼ SE180328ļź╝ race 2ļĪ£ Ļ▓░ļĪĀ ļé┤ļĀĖļŗż(Table 1). ņ¦ĆĻĖłĻ╣īņ¦Ć ĻĄŁļé┤ņØś P. xanthiiņØś Ļ▓ĮņÜ░ race 2ļĪ£ ļČäļźś ļ│┤Ļ│ĀļÉ£ ņśłĻ░Ć ņŚåņ¢┤ ņāłļĪ£ņÜ┤ raceĻ░Ć ņ£Āņ×ģ Ēś╣ņØĆ ļ│ĆņØ┤ĒĢśĻ│Ā ņ׳ņØīņØä ņŗ£ņé¼ĒĢśņśĆļŗż.
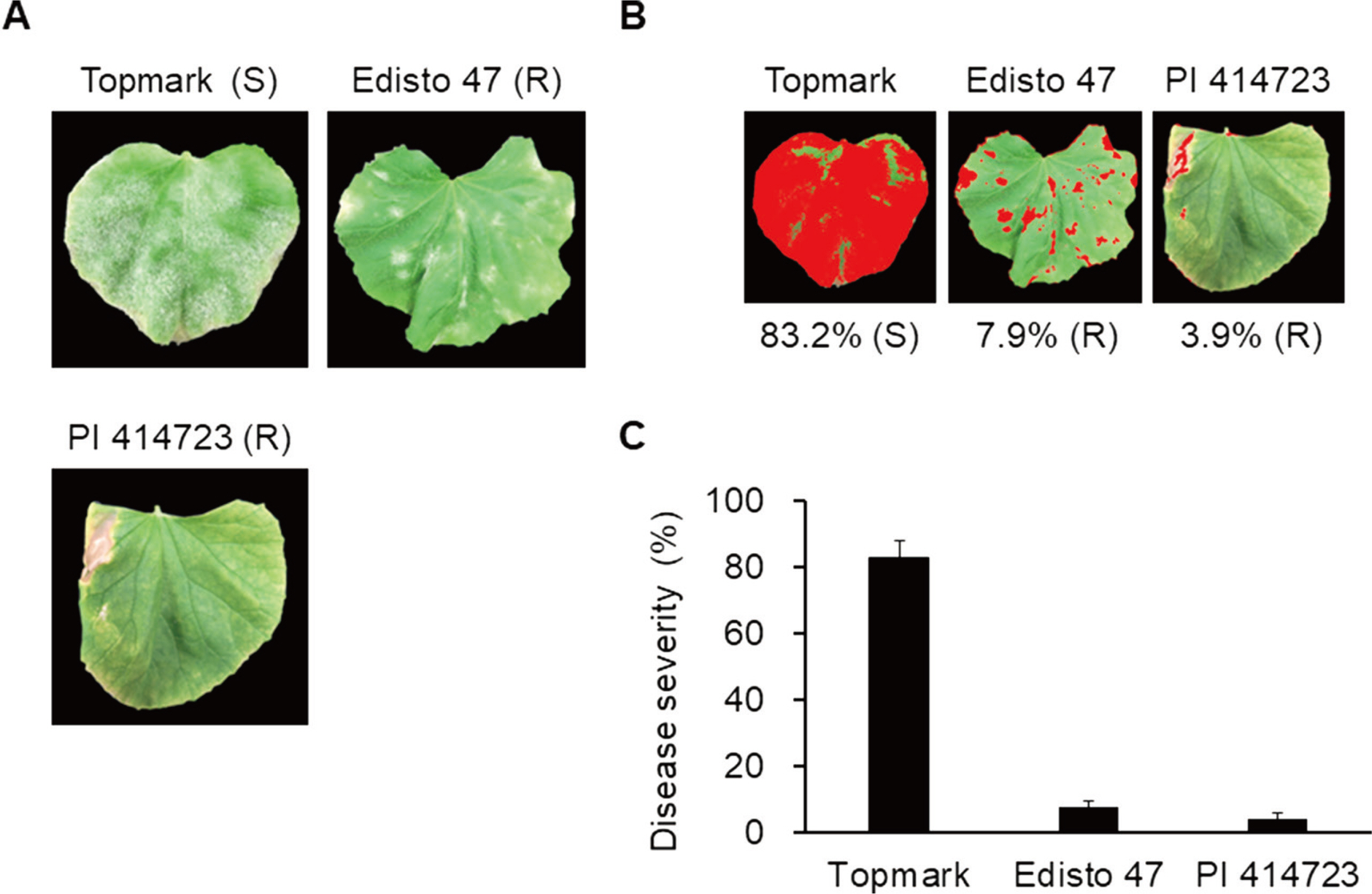
P. xanthii race 1Ļ│╝ race 2ņØś ļ│ĆņØ┤ņ▓┤(variants)ņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼ļź╝ ļ│┤ļ®┤ race 1ņŚÉņä£ 8Ļ░£ņØś ļ│ĆņØ┤ņ▓┤ņÖĆ race 2ņŚÉņä£ 6Ļ░£ņØś ļ│ĆņØ┤ņ▓┤Ļ░Ć ļ│┤Ļ│ĀļÉśņ¢┤ ņ׳ļŗż(Cohen ļō▒, 2004; McCreight, 2006). Race 2ņØś ļ│ĆņØ┤ņ▓┤ņØĖ 2aņÖĆ 2bņØś Ļ▓ĮņÜ░ ņĢäņ¦ü ļ¬ģĒÖĢĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ļÉśņ¦Ć ņĢŖņĢä ļŗżļźĖ ļ│ĆņØ┤ņ▓┤ņÖĆ ļÅÖņØ╝ĒĢĀ Ļ░ĆļŖźņä▒ņØ┤ ņĀ£ĻĖ░ļÉśĻ│Ā ņ׳ļŗż(Cohen ļō▒, 2000; McCreight, 2006). ņĄ£ĻĘ╝ņŚÉļŖö 10Ļ░£ņØś ļ®£ļĪĀ ĒīÉļ│ä ņŗØļ¼╝ņØä ņØ┤ņÜ®ĒĢśņŚ¼ race 2ļź╝ 2S (Salinas), 2US(United States), 2F (France), 2SC (South Carolina)ļĪ£ ļČäļźśĒĢśņśĆļŗż(Tetteh ļō▒, 2013). ļ»ĖĻĄŁņŚÉņä£ļŖö P. xanthii race 2USĻ░Ć ņłśļ░ĢņŚÉņä£ ņóĆ ļŹö ļ¦ÄņØĆ Ēö╝ĒĢ┤ļź╝ ņØ╝ņ£╝ĒéżļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņŚłņ£╝ļ®░(Davis ļō▒, 2007; Tetteh ļō▒, 2013), ņżæĻĄŁņŚÉņä£ļŖö ļ®£ļĪĀņŚÉ ĒØ░Ļ░ĆļŻ©ļ│æņØä ņØ╝ņ£╝ĒéżļŖö ņŻ╝ņÜö P. xanthiiĻ░Ć race 2Fņ×äņØ┤ ļ░ØĒśĆņĀĖ(Wang ļō▒, 2006), ĻĄŁĻ░Ćļ│äļĪ£ ņ×æļ¬®ļ│äļĪ£ Ļ░üĻĖ░ ņāüņØ┤ĒĢ£ raceĻ░Ć ņÜ░ņĀÉĒĢśĻ│Ā ņ׳ļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ļŗż. ņØ┤ņŚÉ ĻĖ░ņĪ┤ņØś ņŚ░ĻĄ¼ļōżņØä(Cosme ļō▒, 2012; McCreight, 2006; Tetteh ļō▒, 2013) ļö░ļØ╝ņä£ ņČöĻ░ĆņĀüņØĖ ļ®£ļĪĀ ĒīÉļ│ä ņŗØļ¼╝ņØĖ ŌĆśEdisto 47ŌĆÖņÖĆ ŌĆśPI 414723ŌĆÖņØä ņØ┤ņÜ®ĒĢśņŚ¼ SE180328Ļ░Ć race 2ņØś ļ│ĆņØ┤ņ▓┤ņØĖ 2S, 2US, 2F, 2SC ņżæņŚÉņä£ ņ¢┤ļ¢ż raceņØĖņ¦Ćļź╝ ņĪ░ņé¼ĒĢśņśĆļŗż(Fig. 5). TopmarkļŖö ņŚ¼ņĀäĒ׳ ļåÆņØĆ Ļ░Éņłśņä▒(83.2%)ņØä ļ│┤ņśĆņ£╝ļéś ŌĆśEdisto 47ŌĆÖņÖĆ ŌĆśPI 414723ŌĆÖņØĆ Ļ░üĻ░ü 7.9%ņÖĆ 3.9%ļĪ£ ļ¬©ļæÉ ļåÆņØĆ ņłśņżĆņØś ņĀĆĒĢŁņä▒ņØä ļéśĒāĆļāłļŗż. ņØ┤ļź╝ ļ░öĒāĢņ£╝ļĪ£ SE180328ļŖö P. xanthii race 2FļĪ£ ņĄ£ņóģ Ļ▓░ļĪĀĒĢśņśĆļŗż(Table 1).
ĒØ░Ļ░ĆļŻ©ļ│æ(powdery mildew)ņØĆ ņśżņØ┤(Cucumis sativus)ļź╝ ĒżĒĢ©ĒĢśļŖö ļ░ĢĻ│╝(Cucurbitaceae) ņ×æļ¼╝ņŚÉņä£ ņĀä ņäĖĻ│äņĀüņ£╝ļĪ£ Ļ░Ćņן ņŗ¼Ļ░üĒĢ£ Ēö╝ĒĢ┤ļź╝ ņØ╝ņ£╝ĒéżļŖö ņŻ╝ņÜöĒĢ£ ļ│æ ņżæ ĒĢśļéśņØ┤ļŗż. ņśżņØ┤ ĒØ░Ļ░ĆļŻ©ļ│æņØś ņ¦ĆņåŹņĀüņØĖ ļ░£ļ│æĻ│╝ ļ░®ņĀ£ņØś ņ¢┤ļĀżņøĆ ļĢīļ¼ĖņŚÉ ĻĘĖ ņøÉņØĖ ļ│æņøÉĻĘĀņØä ļ░ØĒ׳Ļ│Ā raceļź╝ ĻĘ£ļ¬ģĒĢśļŖö Ļ▓āņØ┤ ĒĢäņłśņĀüņØ┤ļŗż. ĻĄŁļé┤ņŚÉņä£ ļ░£ļ│æĒĢśļŖö ņśżņØ┤ ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀņØś ņĪ░ņé¼ļź╝ ņ£äĒĢśņŚ¼ Ļ▓ĮĻĖ░ļÅä Ļ┤æņŻ╝(Gwangju), Ļ▓ĮĻĖ░ļÅä ņØ┤ņ▓£(Icheon), ņĀäļØ╝ļČüļÅä Ļ╣ĆņĀ£(Gimje), ņä£ņÜĖĒŖ╣ļ│äņŗ£(Seoul), Ļ▓Įņāüļé©ļÅä ļ░Ćņ¢æ(Miryang) ņ¦ĆņŚŁņŚÉņä£ ĒØ░Ļ░ĆļŻ©ļ│æņØ┤ ļ░£ņāØĒĢ£ ņśżņØ┤ ņ×ÄņØä ņ▒äņ¦æĒĢśņśĆļŗż. ĒśĢĒā£ĒĢÖņĀü, ļČäņ×ÉņāØļ¼╝ĒĢÖņĀü ĒŖ╣ņä▒ ņĪ░ņé¼ Ļ▓░Ļ│╝ ļČäļ”¼ļÉ£ ņśżņØ┤ ĒØ░Ļ░ĆļŻ©ļ│æĻĘĀļōżņØĆ ņĀłļīĆ ĒÖ£ļ¼╝ĻĖ░ņāØĻĘĀņØĖ Podosphaera xanthiiļĪ£ ļÅÖņĀĢļÉśņŚłļŗż. P. xanthiiņØś race ĻĘ£ļ¬ģņŚÉ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŖö ļ®£ļĪĀ(C. melo) ĒīÉļ│ä ĒÆłņóģņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļ░Ćņ¢æ, ņØ┤ņ▓£ ņä£ņÜĖņŚÉņä£ ļČäļ”¼ļÉ£ MI180427, IC190611, SE180328ņØś ļĀłņØ┤ņŖżļź╝ Ļ░üĻ░ü ņĪ░ņé¼ĒĢśņśĆļŗż. ļČäļ”¼ĻĘĀņŻ╝ MI180427Ļ│╝ IC190611ļŖö ĻĄŁļé┤ņŚÉņä£ Ļ░Ćņן Ļ┤æļ▓öņ£äĒĢśĻ▓ī ļ░£ļ│æļÉśĻ│Ā ņ׳ļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉ£ race 1ņ£╝ļĪ£ ĻĘ£ļ¬ģļÉśņŚłļŗż. ļ░śļ®┤, ļČäļ”¼ĻĘĀņŻ╝ SE180328ļŖö ĻĄŁļé┤ņŚÉņä£ ņĢäņ¦üĻ╣īņ¦Ć ļ│┤Ļ│ĀļÉ£ ņśłĻ░Ć ņŚåļŖö race 2ļĪ£ ĒīÉļ│äļÉśņŚłļŗż. SE180328ņØś ņĀĢĒÖĢĒĢ£ race ĒīÉļ│äņØä ņ£äĒĢ┤ņä£ ņČöĻ░ĆņĀüņØĖ ļ®£ļĪĀ ĒīÉļ│ä ĒÆłņóģņŚÉ ņĀæņóģĒĢ£ Ļ▓░Ļ│╝, ĒØ░Ļ░ĆļŻ©ļ│æ race 2 ņżæņŚÉņä£ ņżæĻĄŁ ļ▓ĀņØ┤ņ¦ĢņØś ņŻ╝ņÜö raceļĪ£ ņĢīļĀżņ¦ä race 2FļĪ£ ļÅÖņĀĢļÉśņŚłļŗż. ļö░ļØ╝ņä£ ņāłļĪ£ņÜ┤ race 2FņØś ĻĄŁļé┤ ļ░£ļ│æņØä ļ│┤Ļ│ĀĒĢśļŖö ļ│Ė ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ļŖö Ē¢źĒøä ņśżņØ┤ ĒØ░Ļ░ĆļŻ©ļ│æ ņĀĆĒĢŁņä▒ ĒÆłņóģ ņ£Īņä▒ņŚÉ Ļ│ĀļĀż ļÉśņ¢┤ņĢ╝ ĒĢĀ ĻĖ░ņ┤łņ×ÉļŻīĻ░Ć ļÉĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
Acknowledgments
This study was carried out with the support of ╩╗╩╗Cooperative Research Program for Agriculture Science & Technology Development (Project No. PJ01421303)ŌĆÖŌĆÖ Rural Development Administration, Republic of Korea
Fig.┬Ā1
Regional distribution and photographs of powdery mildew isolated from cucumber (Cucumis sativus) in Korea. (A) Five locations where samples were harvested in Korea. (B) Cucumber leaf samples displaying typical powdery mildew symptom from five different locations. 1, Gimje (isolate KI170723); 2, Gwangju (isolate GW170710); 3, Seoul (isolate SE180328); 4, Miryang (isolate MI180427); 5, Icheon (isolate IC190611). (C) Conidia spore of Podosphaera xanthii isolates. Scale bars=50 ╬╝m.

Fig.┬Ā2
Inoculation of four melon differentials (Cucumis melo cv. Topmark, PMR 45, PMR 6, and MR-1) with Podosphaera xanthii isolate MI180427. (A) Representative images of leaf disks 12 days after inoculation. S, susceptible; R, resistance. (B) Representative images using disease severity analysis with ImageJ software. (C) Disease severity of four melon differentials. Data are shown as relative lesion area compared to the leaf disk. Experiments were performed in at least triplicate and repeated three times with similar results.

Fig.┬Ā3
Inoculation of four melon differentials (Cucumis melo cv. Topmark, PMR 45, PMR 6, and MR-1) with Podosphaera xanthii isolate IC190611. (A) Representative images of leaf disks 12 days after inoculation. S, susceptible; R, resistance. (B) Representative images using disease severity analysis with ImageJ software. (C) Disease severity of four melon differentials. Data are shown as relative lesion area compared to the leaf disk. Experiments were performed in at least triplicate and repeated three times with similar results.
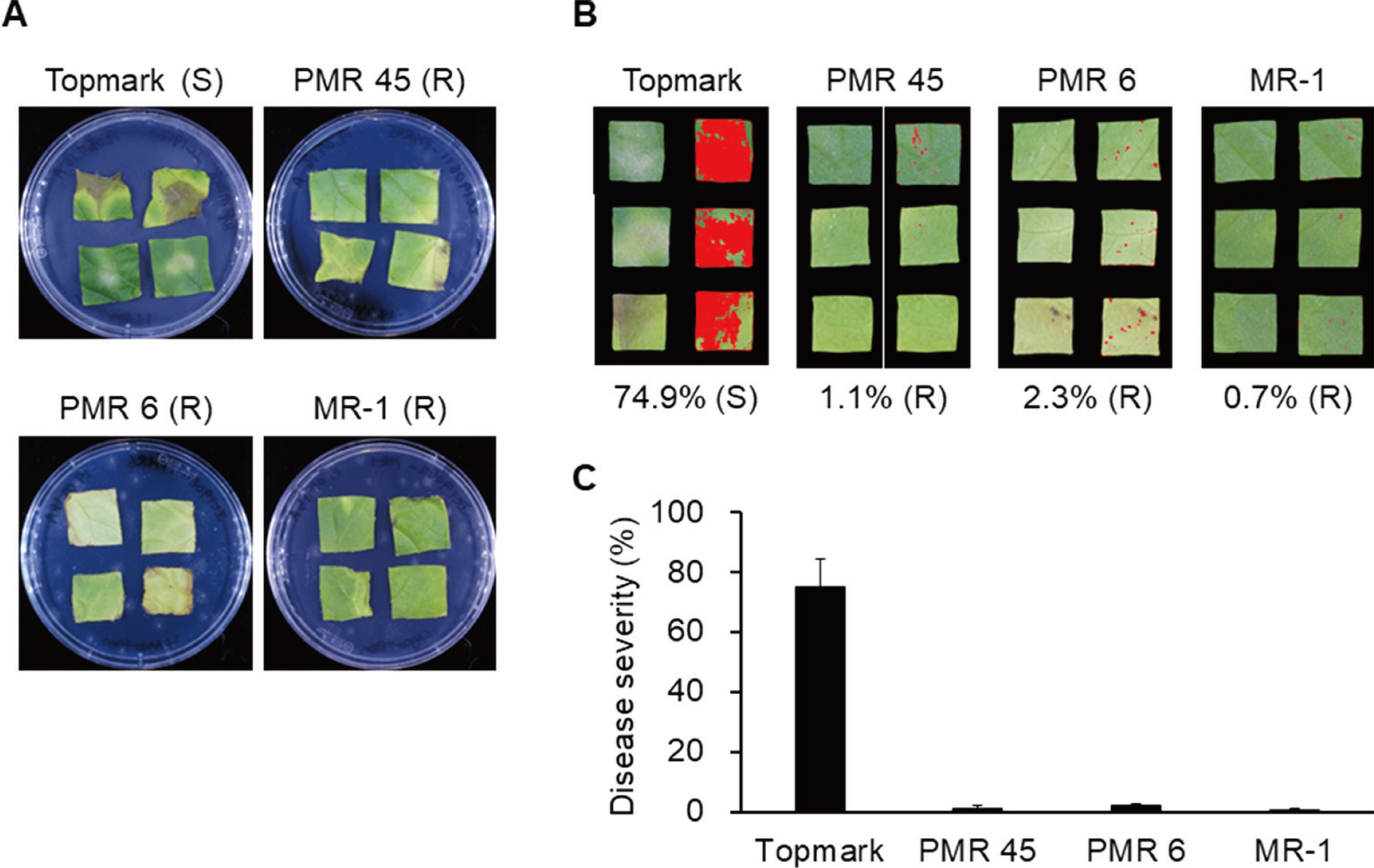
Fig.┬Ā4
Inoculation of four melon differentials (Cucumis melo cv. Topmark, PMR 45, PMR 6, and MR-1) with Podosphaera xanthii isolate SE180328. (A) Representative images of leaf disks 12 days after inoculation. S, susceptible; R, resistance. (B) Representative images using disease severity analysis with ImageJ software. (C) Disease severity of four melon differentials. Data are shown as relative lesion area compared to the whole leaf. Experiments were repeated three times with similar results.
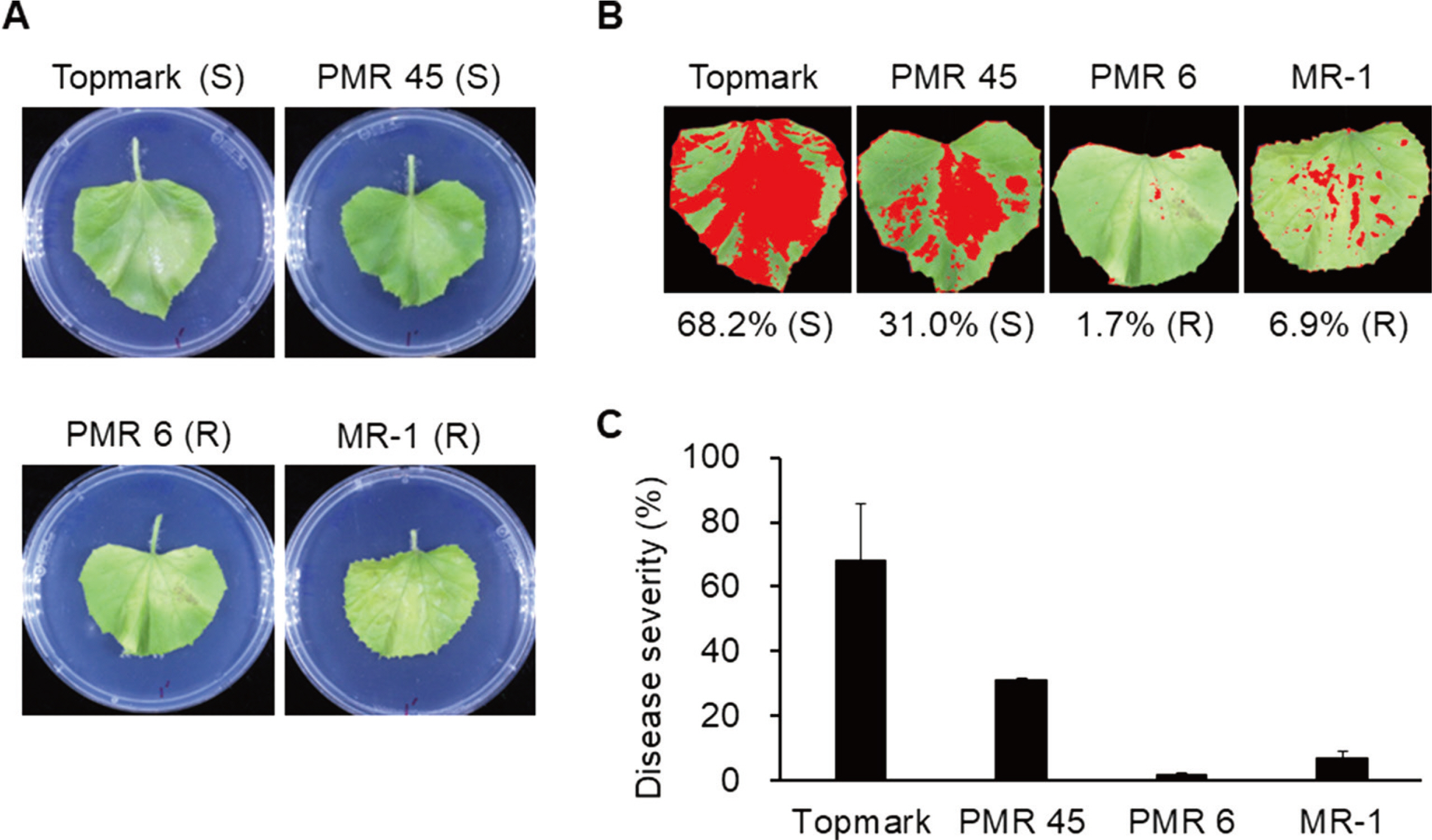
Fig.┬Ā5
Inoculation of additional melon differentials (Edisto 47 and PI 414723) and susceptible control (Topmark) with Podosphaera xanthii isolate SE180328. (A) Representative images of leaves 20 days after inoculation. S, susceptible; R, resistance. (B) Representative images using disease severity analysis with ImageJ software. (C) Disease severity of melon differentials. Data are shown as relative lesion area compared to the whole leaf. Experiments were repeated two times with similar results.
Table┬Ā1
Expected disease reaction and summary of reactions of melon cultigens to Podosphaera xanthii races based on previous reports and present results
| Differentials | Previous reportsa | Present results | |||||||
|---|---|---|---|---|---|---|---|---|---|
|
|
|
||||||||
| Race 1 | Race 2 | Race 3 | MI 180427 | IC 190611 | SE 180328 | ||||
|
|
|||||||||
| 2S | 2US | 2F | 2SC | ||||||
| Tapmark | S | S | S | S | S | S | S | S | S |
| PMR 45 | R | S | S | S | S | S | R | R | S |
| PMR 6 | R | R | R | R | R | S | R | R | R |
| MR-1 | R | R | R | R | R | R | R | R | R |
| Edisto 47 | - | S | S | R | R | - | - | - | R |
| PI 414723 | - | R | S | R | S | - | - | - | R |
References
Bertrand, F. and Pitrat, M. 1989. Screening of a muskmelon germplasm for susceptibility to 5 pathotypes of powdery mildew. Proc. Cucurbitaceae 89: 140-142.
Cohen, Y., Baider, A., Petrov, L., Sheck, L. and Voloisky, V. 2000. Crossinfectivity of Sphaerotheca fuliginea to watermelon, melon, and cucumber. Acta Hortic 510: 85-88.

Cohen, R., Burger, Y. and Katzir, N. 2004. Monitoring physiological races of Podosphaera xanthii (syn.Sphaerotheca fuliginea), the causal agent of powdery mildew in cucurbits: factors affecting race identification and the importance for research and commerce. Phytoparasitica 32: 174-183.

Cosme, B.-R., Josefina, L.-F., Raul, A.-M., Dolores, M.-R. M., Armando, C.-F. J., Benigno, V-T. J. et al. 2012. Characterization of powdery mildew in cucumber plants under greenhouse conditions in the Culiacan Valley, Sinaloa, Mexico. Afr. J. Agric. Res 7: 3237-3248.

Davis, A. R., Levi, A., Tetteh, A., Wehner, T., Russo, V. and Pitrat, M. 2007. Evaluation of watermelon and related species for resistance to race 1W powdery mildew. J. Am. Soc. Hortic. Sci 132: 790-795.

Fanourakis, N. E. 1991. Screening procedures for powdery mildew resistance in the cucumber. Acta Hortic 287: 147-154.

Gafni, A., Calderon, C. E., Harris, R., Buxdorf, K., Dafa-Berger, A., Zeilinger-Reichert, E. et al. 2015. Biological control of the cucurbit powdery mildew pathogen Podosphaera xanthii by means of the epiphytic fungus Pseudozyma aphidis and parasitism as a mode of action. Front. Plant Sci 6: 132



Hong, Y.-J., Hossain, M. R., Kim, H.-T., Park, J.-I. and Nou, I.-S. 2018. Identification of two new races of Podosphaera xanthii causing powdery mildew in melon in South Korea. Plant Pathol. J 34: 182-190.



Hosoya, K., Narisawa, K., Pitrat, M. and Ezura, H. 1999. Race identification in powdery mildew (Sphaerotheca fuliginea) on melon (Cucumis melo) in Japan. Plant Breed 118: 259-262.

Huang, X. Q., Hsam, S. L. K., Zeller, F. J., Wenzel, G. and Mohler, V. 2000. Molecular mapping of the wheat powdery mildew resistance gene Pm24 and marker validation for molecular breeding. Theor. Appl. Genet 101: 407-414.

Jagger, I. C., Whitaker, T. W. and Porter, D. R. 1938. A new biologic form of powdery mildew on muskmelons in the Imperial Valley of California. Plant Dis. Rep 22: 275-276.
Kim, H.-T., Park, J.-I., Ishikawa, T., Kuzuya, M., Horii, M., Yashiro, K. et al. 2015. Development of molecular marker to select resistant lines and to differentiate the races related to powdery mildew in melon (Cucumis melo L.). J. Plant Biotechnol 42: 284-289. (In Korean)

Kim, H.-T., Park, J.-I. and Nou, I.-S. 2016. Identification of fungal races that cause powdery mildew in melon (Cucumis melo L.) and selection of resistant commercial melon cultivars against the identified races in Korea. J. Plant Biotechnol 43: 58-65. (In Korean)

Kuzuya, M., Yashiro, K., Tomita, K. and Ezura, H. 2006. Powdery mildew (Podosphaera xanthii) resistance in melon is categorized into two types based on inhibition of the infection processes. J. Exp. Bot 57: 2093-2100.


Lee, J. H., Jang, K. S., Lee, W. J., Choi, Y. H. and Choi, G. J. 2014. Resistance of cucurbits to Podosphaera xanthii race 1. Korean J. Hortic. Sci. Technol 32: 673-683. (In Korean)

Lee, Y.-H., Seo, J.-B., Choi, K. J., Park, I.-J. and Yang, W.-M. 2004. Disease resistance test method of cucumber powdery mildew (Sphaerotheca fusca) using a leaf disk assay. Res. Plant Dis 10: 78-81. (In Korean)

McCreight, J. D. 2006. Melon-powdery mildew interactions reveal variation in melon cultigens and Podosphaera xanthii races 1 and 2. J. Am. Soc. Hortic. Sci 131: 59-65.

Pirondi, A., Vela-Corcia, D., Dondini, L., Brunelli, A., Perez-Garcia, A. and Collina, M. 2015. Genetic diversity analysis of the cucurbit powdery mildew fungus Podosphaera xanthii suggests a clonal population structure. Fungal Biol 119: 791-801.


Porebski, S., Bailey, L. G. and Baum, B. R. 1997. Modification of a CTAB DNA extraction protocol for plants containing high polysaccharide and polyphenol components. Plant Mol. Biol. Rep 15: 8-15.

Pryor, D. E., Whitaker, T. W. and Davis, G. N. 1946. The development of powdery mildew resistant cantaloupes. Proc. Am. Soc. Hortic. Sci 47: 347-356.
Rabelo, H. O., Santos, L. S., Diniz, G. M. M., Marin, M. V., Braz, L. T. and McCreight, J. D. 2017. Cucurbits powdery mildew race identity and reaction of melon genotypes. Pesq. Agropec. Trop 47: 440-447.
Tetteh, A. Y., Wehner, T. C. and Davis, A. R. 2013. Inheritance of resistance to the new race of powdery mildew in watermelon. Crop Sci 53: 880-887.

Wang, J., Gong, G., Guo, S., Wang, Q. and Xu, Y. 2006. Identification of physiological races of powdery mildew on cucurbits in Beijing. China Veg 8: 7-9.
Zitter, T. A., Hopkins, D. L. and Thomas, C. E. eds. by M. T. McGrath and C. E. Thomas, 1996. Powdery mildew. In: Compendium of Cucurbit Diseases, American Phytopathological Society Press, St. Paul, MN, USA. pp. 28-30.
- TOOLS
-
METRICS

- Related articles
-
Occurrence of Gray Mold in Mango Caused by Botrytis cinerea in Korea2023 September;29(3)



 PDF Links
PDF Links PubReader
PubReader Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print