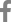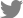요 약
후자린산은 Fusarium이 생성하는 독소로서 다른 Fusarium 독소와 함께 독성을 증진시킬 수 있다. 후자린산 독소를 특이적으로 검출하기 위해 후자린산의 생합성유전자 중 전사인자인 FUB10을 증폭하는 프라이머를 제작하였다. Fub10-f와 Fub10-r 프라이머쌍으로 PCR을 수행했을 때, F. oxysporum, F. proliferatum, F. verticillioides, F. anthophilum, F. bulbicola, F. circinatum, F. fujikuroi, F. redolens, F. sacchari, F. subglutinans, F. thapsinum 에서 약 550 bp의 단일밴드가 증폭되었으며 이들은 모두 후자린산을 생성하는 것으로 알려졌다. 반면 트라이코쎄신을 생성 하는 종에서는 FUB10 특이 밴드가 증폭되지 않았다. 후자린산 은 푸모니신을 생성하는 종에서 함께 생성될 수 있기 때문에 FUB10 프라이머와 푸모니신 생합성유전자인 FUM1 프라이머를 이용한 multiplex PCR을 수행하였다. 그 결과 푸모니신 생성 종인 F. proliferatum과 F. verticillioides에서 밴드가 모두 증폭되었으며 이는 두 가지 독소를 생성할 수 있는 종에서 동시 검출 이 가능함을 시사하였다.
ABSTRACT
Fusaric acid is a mycotoxin produced by species of the fungus Fusarium and can act synergistically with other Fusarium toxins. In order to develop a specific detection method for fusaric acid-producing fungus, PCR primers were designed to amplify FUB10, a transcription factor gene in fusaric acid biosynthetic gene cluster. When PCR with Fub10-f and Fub10-r was performed, a single band (~550 bp) was amplified from F. oxysporum, F. proliferatum, F. verticillioides, F. anthophilum, F. bulbicola, F. circinatum, F. fujikuroi, F. redolens, F. sacchari, F. subglutinans, and F. thapsinum, all of which were known for fusaric acid production. Whereas the FUB10 specific band was not amplified from Fusarium species known to be trichothecene producer. Because production of fusaric acid can co-occur in species that also produce fumonisin mycotoxins, we developed a multiplex PCR assay using the FUB10 primers as well as primers for the fumonisin biosynthetic gene FUM1. The assay yielded amplicons from fumonisin producers such as F. proliferatum and F. verticillioides, allowing for the simultaneous detection of species with the genetic potential to produce both types of mycotoxins.
후자린산(5-butylpicolinic acid, fusaric acid, FA)은
Fusarium 이 생성하는 약독성의 곰팡이독소로서 다른
Fusarium 독소와 중복오염 시 독성증진효과를 보이는 물질로 주목받고 있다 (
Bacon 등, 1995;
Desjardins, 2006). FA는 오랫동안 식물의 시들음병에 관여하는 것으로 알려졌다(
Gaumann, 1957). FA와 병원성 관련성은 명확한 증거가 없었으나 최근 미국에 유입된 새로운 병원형(pathotype)
F. oxysporum 균주는 다량의 FA를 생성하며 이것이 목화의 병원성과 관련 있음이 보고되었다(
Liu 등, 2011a;
2011b). 또한 선인장 유래
F. oxysporum은 FA를 생성하며 기주 선인장에 병을 일으켰다(
Brown 등, 2015). 한편 FA를 생산하는
Fusarium 종으로는
F. verticillioides, F. crookwellense, F. subglutinans, F. sambucinum, F. napiforme, F. oxysporum, F. solani, F. proliferatum, F. fujikuroi 등이 보고되었다(
Bacon 등, 1996;
Niehaus 등, 2014). 이들 중 일부는 푸모니신(fumonisin) 을 생성하는 종으로서 FA의 독성증진효과는 푸모니신이 자주 발생하는 옥수수 등의 작물에서 문제가 될 수 있으나 아직까지 FA의 중복오염 여부는 연구된 바 없었다.
FA 독소의 생합성은 밝혀진 것이 거의 없다가 2012년 최초로 FA 생합성 유전자군이 보고된 후, F. fujikuroi,
F. verticillioides, F. oxysporum에서 FA 생합성 유전자들이 클러스터(cluster)로 존재함이 보고되었다(
Brown 등, 2012;
2015;
Niehaus 등, 2014). 이에 FA 생합성 유전자 12개 중 핵심 전사인자 유전자인
FUB10 의 유전정보를 활용하여
FUB10 특이 프라이머를 제작하였고 FA 생성 종(species)의 특이적 검출에 사용하였다. 또한 이 프라이머쌍을 이용하여 푸모니신 생성종에서 푸모니신과 FA의 중복오염 동시 진단 가능성을 조사하였다.
실험에 사용한
Fusarium 균주는 농과원 보유 또는 후자리움 워크샵(Fusarium Laboratory Workshop)에서 분양받은 균주 (KSU 번호)를 사용하였다(
Table 1). 곰팡이 게놈 DNA의 분리를 위해 감자한천배지(PDA)에서 5일간 배양한 균사체를 긁어 1.5 ml 튜브에 넣은 후 분쇄버퍼(EDTA 20mM, Tris-Cl 100 mM, NaCl 8.19%) 400 μl를 추가하고 pellet pestle을 장착한 드릴로 균사체를 분쇄하였다. 이후 phenol: chloroform: isoamylalcohol (25:24:1)액을 동량 넣고 vortex 한 후 4°C 12000 rpm에서 10분간 원심분리하여 DNA를 분리하였다. DNA가 포함된 상층액은 새 튜브에 옮긴 후 이소프로판올(isopropanol)을 상층 액과 동량으로 추가하여 위아래로 섞고 위의 조건으로 원심분리하여 DNA를 침전시켰다. 침전된 DNA는 70% 에탄올로 세척하여 건조시킨 후 TE 버퍼에 용해하여 4°C에 보관하였다.
Table 1
List of Fusarium isolates tested in this study. FUB10 amplification or fusaric acid (FA) production were marked as + for positive, or - for negative
|
No. |
Isolate |
Species |
FUB10 |
FA productiona
|
|
1 |
Foxy20 |
F. oxysporum
|
+ |
+ |
|
2 |
Fp |
F. proliferatum
|
+ |
+ |
|
3 |
Fv |
F. verticillioides
|
+ |
+ |
|
4 |
KSU 11560 |
F. anthophilum
|
+ |
+ |
|
5 |
KSU 10759 |
F. bulbicola
|
+ |
+ |
|
6 |
KSU H-10847 |
F. circinatum
|
+ |
+ |
|
7 |
KSU C-1993 |
F. fujikuroi
|
+ |
+ |
|
8 |
KSU 18979 |
F. redolens
|
+ |
+ |
|
9 |
KSU B-3852 |
F. sacchari
|
+ |
+ |
|
10 |
KSU E-0990 |
F. subglutinans
|
+ |
+ |
|
11 |
KSU F-4093 |
F. thapsinum
|
+ |
+ |
|
12 |
KSU 11451 |
F. crookwellense
|
- |
+ |
|
13 |
KSU 11427 |
F. culmorum
|
- |
- |
|
14 |
KSU 20979 |
F. equiseti
|
- |
- |
|
15 |
KSU 11470 |
F. poae
|
- |
- |
|
16 |
KSU 11552 |
F. sporotrichioides
|
- |
- |
|
17 |
KSU Z-3639 |
F. graminearum
|
- |
- |
|
18 |
SCK04 |
F. asiaticum
|
- |
- |
후자린산의 생성능 진단을 위해 5종의 FA 생성
Fusarium으로부터 후자린산 생합성에 관련된 유전자 중 전사 인자(transcription factor)인
FUB10 유전자 부위의 염기서열을 확보하고 정렬한 후 정방향 프라이머 Fub10-F(5’-GATTTCATSGTCAATGAMAATATC- 3’, Tm 49°C)와 역방향 프라이머 Fub10-R(5’- TTGAGAAWATGATACCATAGATTG-3’, Tm 49°C)를 제작하였다 (
Fig. 1). 이들 프라이머쌍을 이용해,
Table 1의 균주를 대상으로 Mycycler (Bio-Rad Laboratories, Inc.,CA, 미국)과 TaKaRa Ex Taq(TaKaRa Biotechnology, 일본)을 사용하여 PCR을 실시하였다. 프라이머쌍(10 pM) 및 gDNA(100 ng)를 포함하는 PCR 반응 혼합물 25 μl를 96°C에서 1분 30초간 변성한 후, 94°C에서 30초, 52°C에서 30초, 68°C에서 1분간 반응시키는 싸이클을 35회 실시한 다음, 68°C에서 10분간 반응시켰다.
Fig. 1
Alignment of partial sequences of the FUB10 gene from Fusarium species generated using Clustal W method. Each species name is followed by strain designation. Arrows show the positions and the directions of the Fub10-f/Fub10-r primers. Black shades represent consensus nucleotides among the sequences. Dashes in the middle represent abbreviation of nucleotides between the shown sequences.
PCR 결과, Fub10-F/Fub10-r의 프라이머쌍은
F. oxysporum, F. proliferatum, F. verticillioides, F. anthophilum, F. bulbicola, F. circinatum, F. fujikuroi, F. redolens, F. sacchari, F. subglutinans, F. thapsinum에서 약 550 bp의 단일밴드를 증폭시켰다(F. verticillioides 기준,
Fig. 2). 증폭밴드의 크기는
F. oxysporum, F. proliferatum, F. circinatum, F. fujikuroi, F. redolens 종의 경우
F. verticillioides 보다 1-15 bp 짧았으며
F. anthophilum, F. bulbicola, F. sacchari, F. subglutinans, F. thapsinum 에서는 확인되지 않았다. 그러나 트라이코쎄신을 생성하는
F. crookwellense, F. culmorum, F. equiseti, F. poae, F. sporotrichioides, F. graminearum, F. asiaticum에서는 밴드가 증폭되지 않았다.
F. crookwellense는 FA를 생성하는 것으로 보고된 바 있으나(
Bacon 등, 1996) 이 연구에서는 유전자가 검출되지 않아 기존의 결과가 특정 균주에 국한된 것으로 추정 할 수 있다.
Fig. 2
Amplification of
FUB10 among
Fusarium isolates. Strains corresponding to lanes 1 through 11 can produce fusaric acid. M, 1 kb ladder; C, negative control with water; 1,
F. oxysporum; 2,
F. proliferatum; 3,
F. verticillioides; 4,
F. anthophilum; 5,
F. bulbicola; 6,
F. circinatum; 7,
F. fujikuroi; 8,
F. redolens; 9,
F. sacchari; 10,
F. subglutinans; 11,
F. thapsinum; 12,
F. crookwellense; 13,
F. culmorum; 14,
F. equiseti; 15,
F. poae; 16,
F. sporotrichioides; 17,
F. graminearum; 18,
F. asiaticum. The numbers match to No. in
Table 1.
밴드가 증폭된 종(species) 중,
F. proliferatum, F. verticillioides, F. circinatum, F. fujikuroi, F. sacchari, F. subglutinans, F. thapsinum 은 모두 푸모니신을 생성하는
Fusarium fujikuroi species complex에 속하며 이들이 FA를 생성하는 경우 푸모니신과 FA의 중복오염이 예상된다. 따라서 그 가능성을 푸모니신 생성에 필수적인 생합성유전자
FUM1 유전자(
Proctor 등, 2004)의 동시 증폭을 통해 확인하고자 하였다. 이를 위해 Tm이 낮은 Fub10-f/Fub10-r 프라이머(10 pM) 각각 1 μl,
FUM1 증폭 프라이머 rp32/rp33(10 pM) 각각 0.5 μl를 혼합 사용한 후 위의 기술된
FUB10 PCR과 동일한 조건으로 PCR을 수행하였다. 그 결과, 푸모니신과 FA를 모두 생성하는
F. proliferatum과
F. verticillioides에서는
FUB10 특이 밴드와
FUM1 특이 밴드가 동시에 증폭된 반면 푸모니신을 생성하지 않는
F. oxysporum은 FA 밴드만 증폭되었다 (
Fig. 3). 이것은
FUB10과
FUM1 프라이머의 혼합사용 시, 두 유전자의 동시 검출이 가능함을 증명하는 결과이며 이 두 독소의 중복오염 가능성을 시사한다. 푸모니신과 FA가 동시에 존재할 때 독성이 증가하는 것은 White Leghorn egg에서 보고된 바 있다(
Bacon 등, 1995). 한 종의 균주가 두 가지 이상의 독소를 동시에 생성하는 것은
Fusarium에서 빈번하게 발생한다. 예를 들어, 붉은곰팡이병을 일으키는
F. graminearum이나
F. asiaticum 은 트라이코쎄신인 데옥시니발레놀이나 니발레놀을 생성할 때 이들의 유도체뿐만 아니라 제랄레논을 동시에 생성한다(
Desjardins, 2006). 푸모니신과 FA 생합성유전자가 모두 존재하는
Fusarium에서도 이들 균주들이 실제로 푸모니신과 FA를 동시에 생성하는지 여부와 동시 생성시 독성 증가효과가 있는지는 추후 확인이 필요하다.
Fig. 3
Simultaneous detection of FUB10 and FUM1 in Fusarium proliferatum and F. verticillioides. Identical sets of DNA were tested with different primers: FUB10 only, FUB10 and FUM1, FUM1 only. The white box shows amplification of both FUM1 (upper band) and FUB10 (lower band) by using Fub10-f/Fub10-r and rp32/rp33 primers together. M, 1 kb ladder; 1, negative control without DNA template; 2, F. oxysporum Foxy20; 3, F. proliferatum Fp; 4, F. verticillioides Fv; 5, F. sporotrichioides KSU 11552; 6, F. graminearum KSU Z-3639.

Acknowledgement
This study was carried out with the support of Research Program for Agricultural Science & Technology Development (Project No. PJ008635), National Institute of Agricultural Sciences, Rural Development Administration, Republic of Korea.
References
Bacon, C. W., Porter, J. K. and Norred, W. P. 1995. Toxic interaction of fumonisin B1 and fusaric acid measured by injection into fertile chicken egg.
Mycopathologia 129: 29-35.


Bacon, C. W., Porter, J. K., Norred, W. P. and Leslie, J. F. 1996. Production of fusaric acid by
Fusarium species.
Appl. Environ. Microbiol 62: 4039-4043.




Brown, D. W., Butchko, R. A. E., Busman, M. and Proctor, R. H. 2012. Identification of gene clusters associated with fusaric acid, fusarin, and perithecial pigment production in
Fusarium verticillioides.
Fungal Genet. Biol 49: 521-532.


Brown, D. W., Lee, S.-H., Kim, L.-H., Ryu, J.-G., Lee, S., Seo, Y., Kim, Y. H., Busman, M., Yun, S.-H., Proctor, R. H. and Lee, T. 2015. Identification of a 12-gene fusaric acid biosynthetic gene cluster in
Fusarium species through comparative and functional genomics.
Mol. Plant-Microbe Interact 28: 319-332.


Desjardins, A. E. 2006. Fusarium mycotoxins: chemistry, genetics, and biology. The American Phytopathological Society. St. Paul. Minnesota U.S.A, pp. 260 pp.
Gaumann, E. 1957. Fusaric acid as a wilt toxin. Phytopathology 47: 342-357.
Liu, J., Bell, A. A., Stipanovic, R., Puckhaber, L. and Shim, W. 2011a. A polyketide synthase gene and an aspartate kinase like gene are required for the biosynthesis of fusaric acid in Fusarium f. sp vasinfectum. In: Proceedings of the Beltwide Cotton Conferences. S. Boyd, M. Huffman and B. Robertson Memphis, TN.
Liu, J., Bell, A. A., Wheeler, M. H., Stipanovic, R. D. and Puckhaber, L. S. 2011b. Phylogeny and pathogenicity of
Fusarium oxysporum isolates from cottonseed imported from Australia into California for dairy cattle feed.
Can. J. Microbiol 57: 874-886.


Niehaus, E. M., von Bargen, K. W., Espino, J. J., Pfannmuller, A., Humpf, H. U. and Tudzynski, B. 2014. Characterization of the fusaric acid gene cluster in
Fusarium fujikuroi.
Appl. Microbiol. Biotechnol 98: 1749-1762.



Proctor, R. H., Plattner, R. D., Brown, D. W., Seo, J.-A. and Lee, Y.-W. 2004. Discontinuous distribution of fumonisin biosynthetic genes in the
Gibberella fujikuroi species complex.
Mycol. Res 108: 815-822.








 PDF Links
PDF Links PubReader
PubReader Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print