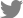|
 |
| Res. Plant Dis > Volume 27(3); 2021 > Article |
|
요 약
2020년 경상북도 포항군 연일읍의 갯기름나물 재배 농가포장에서 잎에 작은 갈색 반점이 형성되고 잎끝부터 갈변되며 고사하는 증상이 발생하였다. 균총은 흰색에서 연한 회색을 띠었다. 균핵은 검은색의 구형 또는 타원형이었다. 자낭반은 컵모양이며, 크기는 0.5‒0.9 cm이었다. 자낭은 원통형이고 크기는75‒240×5.9‒17.3 μm이었다. 자낭포자는 무색의 타원형이었으며 크기는 8.4‒10.7×4.8‒5.8 μm이었다. Internal transcribed spacer (ITS) 1과 ITS4 영역의 염기서열 분석결과 Sclerotinia sclerotiorum과 100% 일치하였으며, 이와 같은 병원균의 균학적 특징, 병원성 검정 결과 그리고 염기서열 분석결과를 바탕으로 갯기름나물 잎반점과 마름 증상의 원인균은 S. sclerotiorum으로 동정하였으며, 이 병을 갯기름나물 균핵병으로 명명할 것을 제안한다.
ABSTRACT
Sclerotinia rot was occurred on the leaf and stem of Peucedanum japonicum Thunb. in greenhouse field of Pohang city of Gyeongbuk province in Korea. The typical symptom of the disease was light brown spot and tipburn on infected leaves. The colony of the isolated fungus was white to light gray in color. Asci were cylindrical shape and 75‒240×5.9‒17.3 μm in size. Apothecia were cup-shaped with numerous asci and 0.5‒0.9 cm in size. Ascospores were aseptate and ellipsoid in shape, and 8.4‒10.7×4.8‒5.8 μm in size. Sclerotia formed on the plants and potato dextrose agar medium were globose to irregular in shape and black in color. Partial sequencing of rDNA of this isolate showed that it was 100% consistent with that of Sclerotinia sclerotiorum. It was confirmed that the same lesion was formed by reinoculating this pathogen on a healthy P. japonicum Thunb. and the same strain was isolated. This is the first report on the Sclerotinia rot of P. japonicum Thunb. caused by S. sclerotiorum in Korea.
갯기름나물의 학명은 Peucedanum japonicum Thunb.이며 생약명으로는 식방풍이라고 명명한다. 이 식물은 한반도를 비롯하여 일본, 중국, 타이완 및 필리핀 등 동아시아의 해안절벽 지형의 토양에서 자생하는 식물이다(Ohwi, 1984). 갯기름나물의 잎은 무딘 톱니 모양이며, 식용나물로 이용된다. 이 식물의 뿌리는 치매 예방(Kim 등, 2013) 등 다양한 인간의 질병 치료효과를 나타내는 성분을 함유하고 있어서 한방재료로 이용된다.
Sclerotinia sclerotiorum은 한국식물병목록에서 국내의 67개 식물에 감염되어 병을 일으키는 것으로 기록되어 있다. 최근 미나리, 들깨, 익모초, 팔손이, 포도나무 등의 식물에 균핵병 발생이 보고되었다(Kwon, 2006; Kwon과 Park, 2002; Kwon 등, 2003; Park 등, 2009, 2017). 국내 갯기름나물에 균핵병 발생이 보고된 예는 없었으나, 2020년 12월에 갯기름나물 재배농가비가림하우스 시설 내에서 잎이 급격하게 마르고 고사되는 증상이 발생하였다. 병반을 형성하는 병원균을 분리하여 형태적 특성과 ribosomal DNA (rDNA)의 internal transcribed spacer(ITS) 염기서열을 분석한 결과를 바탕으로 S. sclerotiorum으로 동정하였다.
병징. 2020년 12월 14일에 경북 포항의 농가 하우스 1동에 서 갯기름나물의 잎이 말라죽는 증상이 발생하였다. 초기에는 잎 전체에 밝은 갈색의 작은 반점이 다수 형성되었으며, 4‒5일 후에는 잎 끝부터 급격하게 말라죽는 특성을 나타내었다.
발생포장 환경조사. 병이 발생한 장소는 폭이 7 m, 길이가 75 m인 단동하우스였으며, 병이 발생한 위치는 하우스 입구에 서 10 m 지점부터 30 m 지점이었다. 하우스 내부에 온습도계를 설치하여 2021년 1월 한 달 동안의 데이터를 수집하였다.
병원균 분리 배양 및 포자형성. 병원균 분리를 위하여 12월 14일에 병징이 나타난 잎과 줄기를 10점 채취하였다. 클린벤치 내에서 병반이 나타난 경계지점을 5×5 cm 크기로 잘라 1% NaClO 용액에 30초 멸균한 후 70% ethanol 용액에 20초 살균 후 멸균수에서 3분간 정치하였다. 시료를 흡습지 올려 5분간 건조 후 water agar 배지에 치상하여 28oC 항온기에서 배양하였다. 72시간 후 자라나오는 균사를 potato dextrose agar (PDA) 배지에 올려 28oC에서 10일간 배양하였다. 또한 자낭포자 형성을 유도하기 위하여 Kwon 등(2003)의 방법을 참조하여 모래 0.3 l를 500 ml 용량의 삼각플라스크에 담아 멸균 후 멸균수를 100 ml 부은 후 균핵을 0.5‒1 cm 깊이로 매몰하였다. 균핵을 묻은 삼각플라스크는 18oC 항온기에서 60일간 배양하며 관찰하였다.
병원성 검정. 분리된 균주의 병원성을 시험하기 위하여 PDA 배지에서 배양한 균사를 3×3 mm 크기로 잘라서 건전한 갯기름나물 잎끝에 치상하였다. 접종처리는 10개의 갯기름나물 잎에 반복 처리하였다. 접종한 잎은 습식처리한 Petri dish 안에 넣어서 28oC로 조절된 항온기에 10일간 보관하며 관찰하였다. 5일에서 10일 경과 사이에 접종한 잎에서 반점이 형성되었으며, 잎 마름 증상의 병반에서 위와 동일한 방법으로 병원균을 분리하였다. 분리한 균주는 처음 접종한 균주와 형태, 균학적 특성 등을 비교하여 동일한 균주임을 확인하였다. 대조구로 water agar 배지의 조각을 치상하였으며, 대조군에서는 병원성반점이 형성되지 않았다.
ITS 염기서열 분석. rDNA의 ITS 염기서열 분석을 위하여 DNA Extraction kit (BIOFACT, Daejeon, Korea)를 이용하여 병원균주의 DNA를 추출하였으며, Solgent (Daejeon, Korea)에 ITS1과 ITS4 영역의 염기서열 분석을 의뢰하였다. 이렇게 얻은 염기서열 자료를 이용하여 NCBI BLAST로 유연관계가 있는 균주들의 ITS rDNA 영역 염기서열을 GenBank에서 수집하였으며 MEGA7을 이용하여 neighbor-joining method로 염기서열을 비교분석하고 phylogenetic tree를 작성하였다.
병징. 갯기름나물 균핵병은 주로 잎 반점과 마름증상을 유발하였고(Fig. 1A, B), 대부분의 뿌리는 건전한 상태이었으나, 매우 드물게 줄기와 뿌리까지 감염된 개채도 관찰되었다(Fig. 1C). 균핵병은 토양전염성 병으로 뿌리썩음과 물러짐 증상을 유발하는 것과 다른 증상을 나타내었다. 균핵병이 잎에 발생한 이유는 자낭포자에 의한 감염이 추정된다. 이러한 병징은 균핵에서 형성된 자낭반의 포자가 비산되고 12월 중순 일교차가 심한 하우스 내부의 습한 환경과 야간에 갯기름나물의 잎에 이슬이 맺히는 조건과 만나면서 병원균이 기공을 통해 침입 감염된 것으로 보인다. 병원균에 감염된 개체는 지제부와 뿌리가 물러지고 말라죽은 줄기 표면에 검은색의 균핵이 형성되기도 하였다(Fig. 1C). 잎 반점 증상은 450 m2 규모의 하우스 내부의 가운데 부분에 100 m2 면적에 집중적으로 발생하였으며, 발병 구역 내의 발병률은 95% 정도였다.
발생환경. 갯기름나물 잎반점과 마름 증상은 2020년 12월부터 2021년 2월까지 포항시 연일읍의 4년생 갯기름나물 재배 농가 시설하우스 내에서 발생하였다. 이 농가는 비닐하우스 야간 보온을 위하여 수막재배 방식을 실시하고 있었다. 2021년 1월의 하우스내 온도와 습도를 측정한 결과 한낮의 최고온도는 30‒44oC였고, 최저 온도는 0‒9oC 정도로 약 30oC 정도 일교차가 발생하였으며, 습도는 100%인 시간이 하루 평균 18시간 이상이었다(Fig. 2). 이 시기의 하우스 내부 평균온도가 12.5oC이었으며, 평균 습도는 90.7%이었다. 갯기름나물의 균핵병이 잎에 국부적으로 대발생하는 현상은 노지 재배지에서는 거의 관찰되지 않는다. 균핵병의 균핵은 평균온도 18oC 정도의 환경에서 적절한 수분이 있을 때 발아하여 자낭반과 자낭포자를 형성한다. 따라서 균핵이 발아하여 12월 중순에 자낭포자가 비산되어 습한 하우스내부의 환경에서 잎에 침입하여 반점과 잎마름 증상을 유발하는 균핵병이 대발생한 것으로 보인다. Hahm 등(2017)이 보고한 바질 균핵병은 비가림하우스 내에 식물체의 줄기와 잎 부분에 대발생한 점이 본 연구에서 분리된 갯기름나물 균핵병 발생 양상과 비슷하였다.
병원균 분리 및 균학적 특성. 반점에서 분리된 병원균은 흰색이나 밝은 잿빛을 띠는 곰팡이였다. PDA 배지에 치상하여 28oC 항온기에서 10일 경과하자 검은색의 균핵이 형성되었다. 균핵의 크기는 1‒3 mm 정도였으며 모양은 구형에서 타원형 형태이었다(Fig. 3A). 병원균의 자낭반은 멸균된 모래에 균핵을 묻어 18oC에 보관한지 45일 경과 시점에 형성되었다. 자낭반의 모양은 자루가 가늘고 길며 머리 부분은 컵모양으로 지름이 0.5‒0.9 cm 크기였다(Fig. 3B). 자낭은 원통형으로 크기는 75‒240×5.9‒17.3 μm이었고, 자낭포자는 타원형의 무색으로 크기는 8.4‒10.7×4.8‒5.8 μm 범위였다(Table 1, Fig. 3C, D). 분리된 병원균의 균학적 특성을 조사한 결과 S. sclerotiorum의 형태적 특성에 부합하였다(Kohn 1979; Udagawa 등, 1980).
병원성 검정. 갯기름나물 균핵병원균의 식물체에 대한 병원성을 확인하기 위하여 건전한 갯기름나물 잎에 접종한 결과, 3일 후 잎에 동일한 병징이 형성되었다(Fig. 1D). 이 감염부위 조직을 표면 살균하여 배지에 배양하여 분리한 결과, 처음 접종한 균주와 동일한 특성을 가지는 균주임을 확인하였다.
염기서열 분석. 이 병원균의 ITS1과 ITS4 영역의 염기서열(515bp)을 nucleotide BLAST로 분석한 결과 S. sclerotiorum (accession no. MT393753.1) 등과 100% 일치하였다. 분리된 갯기름나물 병원균의 ITS 염기서열을 S. sclerotiorum (MK074848) 등 5종과 Sclerotinia minor (MK356550) 등 다른 종의 Sclerotinia속 9종 그리고 Botrytis cinerea 2종의 염기서열을 이용하여 MEGA7으로 phylogenetic tree를 작성한 결과, S. sclerotiorum과 일치하는 것으로 분석되었다(Fig. 4). 갯기름나물 병원균 균주의 ITS 부분 염기서열을 National Center for Biotechnology Information (NCBI)의 Gen-Bank에 등록하였다(accession no. MZ619140). 이 결과를 바탕으로 갯기름나물에 발생한 병은 S. sclerotiorum (isolate Pohang2-1)으로 동정하였으며, 국내에 첫 보고된 갯기름나물 균핵병으로 명명하고자 한다.
Fig. 1.
Symptom and mycelial mats characteristics of Sclerotinia sclerotiorum of Peucedanum japonicum. (A) Early symptoms in fields. (B) Acute onset symptoms. (C) Sclerotia on stem and sheath. (D) Symptoms developed by reinoculating the leaves with pathogen.

Fig. 2.
January temperature and humidity in the green house where Sclerotinia sclerotiorum occurs on Peucedanum japonicum.
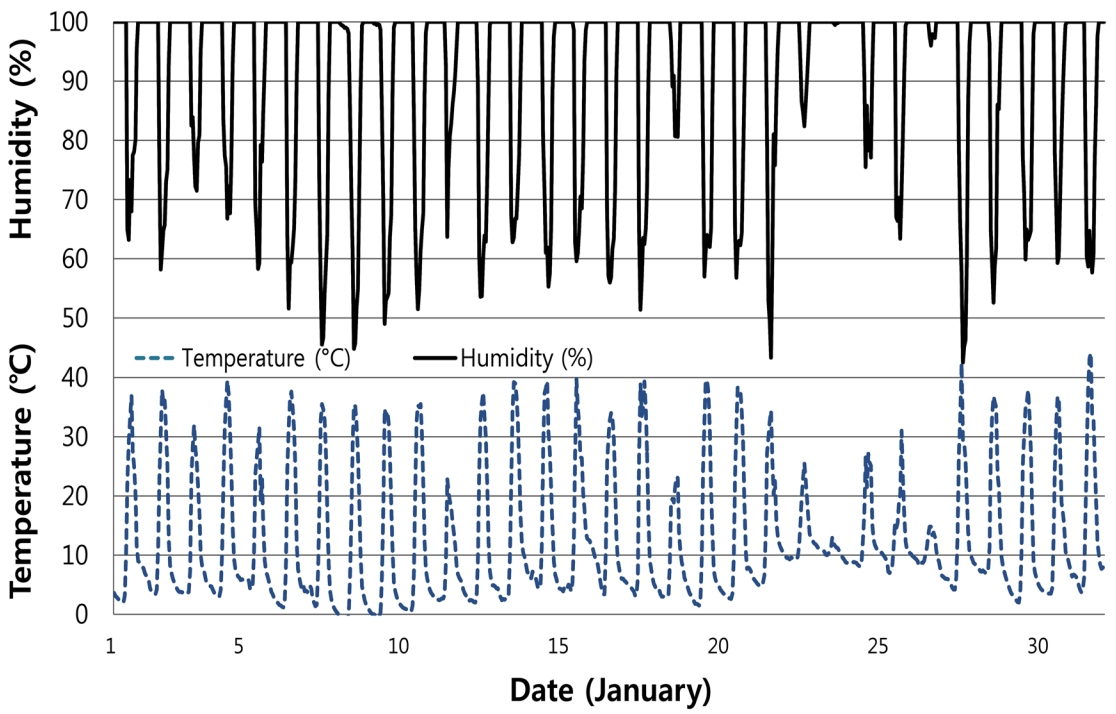
Fig. 3.
Morphological characteristics of Sclerotinia sclerotiorum isolated from Peucedanum japonicum. (A) Mycelial mats. (B) Apothecia produced from sclerotia. (C) Asci. (D) Ascospores.
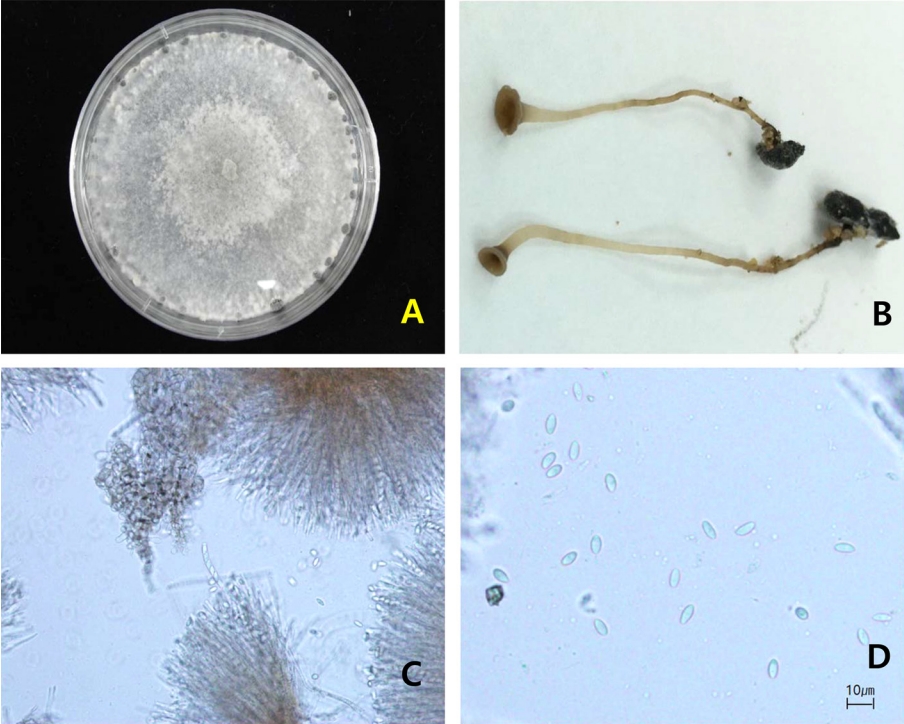
Fig. 4.
Phylogenetic relationship between MZ619140 (Pohang2-1 isolate) and some reference Sclerotinia sp. and Botrytis cinerea isolates retrieved from GenBank, inferred by neighbor-joining method using the internal transcribed spacer rDNA region.

Table 1.
Morphological and cultural characteristics of Sclerotinia sclerotiorum isolated from Peucedanum japonicum
| Characteristics | Present isolate | S. sclerotioruma | |
|---|---|---|---|
| Colony | Color | White-faintly gray | Colorless-chocolate |
| Aporthecium | Shape | Cup-shaped | Cup-shaped |
| Size (cm) | 0.5-0.9 | 0.5-2 | |
| Ascus | Shape | Cylindrical | Cylindrical |
| Size (μm) | 75-240×5.9-17.3 | 80-250×4.5-22.5 | |
| Ascospore | Shape | Ellipsoid | Ellipsoid |
| Size (μm) | 8.4-10.7×4.8-5.8 | 9-13×4-6.5 | |
| Color | Colorless | Colorless | |
| Sclerotium | Color | Black | Black |
| Shape | Globoes, ellipsoid Irregular | Globoes, ellipsoid Irregular | |
References
Hahm, S. S., Kim, B. R., Han, K. S., Kwon, M. K. and Park, I. H. 2017. Sclerotinia rot on basil caused by Sclerotinia sclerotiorum in Korea. Res. Plant Dis. 23: 56-59.

Kim, K.-N., Choi, M.-J., Lee, Y. and Cho, S.-H. 2013. The protective and recovery effects of Peucedanum japonicum Thunberg for vascular dementia. J. Orient. Neuropsychiatry 24: 123-130.

Kohn, L. M. 1979. A monographic revision of the genus Sclerotinia. Mycotaxon 9: 365-444.
Kwon, J.-H. 2006. Sclerotinia rot of Fatsia japonica caused by Sclerotinia sclerotiorum. Res. Plant Dis. 8: 113-116.

Kwon, J.-H. and Park, C.-S. 2002. Occurrence of sclerotinia rot of Leonurus sibiricus caused by Sclerotinia sclerotiorum. Res. Plant Dis. 8: 113-116.

Kwon, J.-H., Shen, S.-S. and Park, C.-S. 2003. Sclerotinia rot of water cress (Oenanthe javanica) caused by Sclerotinia sclerotiorum. Res. Plant Dis. 9: 85-88.

Ohwi, J. 1984. Flora of Japan. Smithsonian Institution, Washington, D.C., USA. 685 pp.
Park, J.-H., Han, K.-S., Han, Y.-K., Lee, J.-S., Kim, D.-H. and Hwang, J.- H. 2009. Sclerotinia shoot rot of grapevine (Vitis spp.) caused by Sclerotinia sclerotiorum in Korea. Res. Plant Dis. 15: 259-261.

Park, M. S., Kim, Y. G., Lee, S. W., Park, C. G., Kim, Y. I., Lee, E. S. et al. 2017. First report of Sclerotinia sclerotiorum causing sclerotinia rot on Ixeridium dentatum in Korea. Korean J. Mycol. 45: 381-385.
Udagawa, S., Tubaki, K., Horie, Y., Miura, K., Minoura, K., Yamazaki, M. et al. 1980. Illustrated Genera of Fungi. Kodansha, Tokyo, Japan. 1321 pp.
- TOOLS
-
METRICS

-
- 0 Crossref
- 0 Scopus
- 2,985 View
- 75 Download
- Related articles
-
White Rot of Korean Wild Chive Caused by Stromatinia cepivora2023 June;29(2)
Shoot Rot of Spikenard Caused by Rhizoctonia solani AG-2-12022 March;28(1)
Post-harvest Green Pea Pod Rot Caused by Sclerotinia sclerotiorum in Korea2022 March;28(1)
Sclerotinia Rot on Basil Caused by
Sclerotinia sclerotiorum in Korea2017 March;23(1)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print